现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl‾、OH‾、NO3‾、CO 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是
(填化学式);
(2)为了确定X,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕灰色沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解,最后留有白色沉淀不再溶解。则:
①X为 ;
A.SO B.SO
B.SO C.CH3COO D.SiO
C.CH3COO D.SiO
②A中的化学键类型为 ;
③将0.02 mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (精确到0.1g);
④利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论 ;
(3)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,则该反应的离子方程式为: 。
自然界中的水要经过消毒杀菌才可成为生活饮用水。ClO2是一种高效安全灭菌消毒剂,
其中Cl化合价为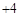 价。
价。
(1)氯原子最外层有 种能量不同的电子,某化合物中O的化合价与ClO2中O的化合价恰好相反,写出该化合物的分子式 。
(2)下列可用作比较S和C非金属性强弱依据的是
A.CS2中各元素的化合价B.气态氢化物的稳定性
C.元素在周期表中的位置 D.最高价含氧酸的酸性
(3)以下性质的比较正确的是
A.键长:HF>HClB.稳定性:HF>HCl
C.酸性:HF>HClD.沸点:HF>HCl
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应① O3 O2 +[O]-Q平衡常数为K1 ;
O2 +[O]-Q平衡常数为K1 ;
反应② [O]+O3 2O2+Q平衡常数为K2 ;
2O2+Q平衡常数为K2 ;
总反应:2O3 3O2+Q平衡常数为K。
3O2+Q平衡常数为K。
(4)一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。
已知:O3的起始浓度为0.0216 mol/L。
| pH t / min T / ℃ |
3.0 |
4.0 |
5.0 |
6.0 |
| 20 |
301 |
231 |
169 |
58 |
| 30 |
158 |
108 |
48 |
15 |
| 50 |
31 |
26 |
15 |
7 |
在30°C、pH=4.0条件下,O3的分解速率为_______________ mol/ (L·min)。
(5)根据表中数据,推测O3在下列条件下分解速率由小到大的顺序为________。(填字母代号)
A.40°C、pH=3.0B.10°C、pH=4.0C.30°C、pH=7.0
(6)下列叙述正确的是
A.降低温度,K增大B.K=K1+K2
C.适当升温,可提高消毒效率 D.压强增大,K2减小
有机物F是一种新型涂料固化剂,可由下列路线合成(部分反应条件略去):
(1)B的结构简式是;E中含有的官能团名称是。
(2)乙烯在实验室可由(填有机物名称)通过(填反应堆类型)制备。
(3)由C和E合成F的化学方程式是。
(4)同时满足下列条件的苯的同分异构体的结构简式是。
①含有3个双键;②分子中只含1种化学环境氢原子;③不存在甲基
(5)下列说法正确的是。
①B属于石油裂解气的主要成分之一②D与乙醛的分子式相同
③E是某种蛋白质水解的最终产物④F可以发生酯化反应
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________________,该反应的类型是________;
(2)写出两种能发生银镜反应的B的同分异构体的结构简式________________________。
(3)C是芳香化合物,相对分子质量180,其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________。
(4)已知C的芳环上有三个取代基。其中一个取代基无支链,且有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是。另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是。
(5)A的结构简式是。
某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子。某小组在实验室中用浸出-萃取法制备硫酸铜: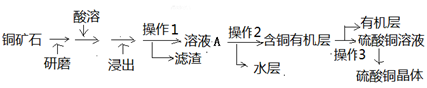
(1)操作1的名称为。操作2用到的玻璃仪器有烧杯和
(2)“浸出”步骤中,为提高铜的浸出率,可采取的措施有
(3)比较操作2之前与操作3之后的溶液,说明两步骤主要目的是。
(4)取少量所得溶液A,滴加(填物质名称)溶液后呈红色,说明溶液中存在Fe3+,检验溶液中还存在Fe2+的方法是(注明试剂、现象)(不考虑除注明外的其它杂质干扰)
(5)用滴定法测定CuSO4·5H2O的含量。取a g试样配成100 mL溶液,取20.00mL用c mol /L 滴定剂(H2Y2–,滴定剂不与杂质反应)滴定至终点,消耗滴定剂bmL.
滴定反应:Cu2+ + H2Y2– CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是。
CuY2–+ 2H+。则CuSO4·5H2O质量分数的表达式是。
(6)下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
A.滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准液至锥形瓶中
B.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定
C.滴定前,滴定管尖端有气泡,滴定后气泡消失
工业生产纯碱的工艺流程示意图如下:
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A、B。
(2)碳酸化后发生反应的化学方程式是 。
(3)向母液(选填图中字母)中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有
A.增大NH4+的浓度,使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(4)不用其它试剂,检查副产品NH4Cl是否纯净的方法及操作是 .
(5)Xg纯碱产品(含有碳酸氢钠)充分加热分解后,质量减少了Yg,则纯碱样品中碳酸氢钠的质量分数可表示为。
(6)有人以硫酸钠和焦炭、石灰石在高温下进行煅烧,再浸取,结晶而制得纯碱。反应的化学方程式为_________ __(已知产物之一为CaS);