自然界中的水要经过消毒杀菌才可成为生活饮用水。ClO2是一种高效安全灭菌消毒剂,
其中Cl化合价为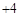 价。
价。
(1)氯原子最外层有 种能量不同的电子,某化合物中O的化合价与ClO2中O的化合价恰好相反,写出该化合物的分子式 。
(2)下列可用作比较S和C非金属性强弱依据的是
A.CS2中各元素的化合价 B.气态氢化物的稳定性
C.元素在周期表中的位置 D.最高价含氧酸的酸性
(3)以下性质的比较正确的是
A.键长:HF>HCl B.稳定性:HF>HCl
C.酸性:HF>HCl D.沸点:HF>HCl
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应① O3 O2 +[O]-Q 平衡常数为K1 ;
O2 +[O]-Q 平衡常数为K1 ;
反应② [O]+O3 2O2+Q 平衡常数为K2 ;
2O2+Q 平衡常数为K2 ;
总反应:2O3 3O2+Q 平衡常数为K。
3O2+Q 平衡常数为K。
(4)一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。
已知:O3的起始浓度为0.0216 mol/L。
| pH t / min T / ℃ |
3.0 |
4.0 |
5.0 |
6.0 |
| 20 |
301 |
231 |
169 |
58 |
| 30 |
158 |
108 |
48 |
15 |
| 50 |
31 |
26 |
15 |
7 |
在30°C、pH=4.0条件下,O3的分解速率为_______________ mol/ (L·min)。
(5)根据表中数据,推测O3在下列条件下分解速率由小到大的顺序为________。(填字母代号)
A.40°C、pH=3.0 B.10°C、pH=4.0 C.30°C、pH=7.0
(6)下列叙述正确的是
A.降低温度,K增大 B.K=K1+K2
C.适当升温,可提高消毒效率 D.压强增大,K2减小
工业制备高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
①KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是______(填代号)。
a、84消毒液(NaClO溶液) b、双氧水 c、苯酚 d、75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______(填代号)。
a、浓硝酸 b、硝酸银 c、氯水 d、烧碱
③上述流程中可以循环使用的物质有、(写化学式)。
④若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得mol KMnO4。
⑤该生产中需要纯净的CO2气体。若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)。a、石灰石 b、稀HCl c、稀H2SO4 d、纯碱
⑥操作Ⅰ的名称是;操作Ⅱ根据KMnO4和K2CO3两物质在(填性质)上的差异,采用(填操作步骤)、趁热过滤得到KMnO4粗晶体。
(1)化学实验必须注意安全,下列做法存在安全隐患的是(选填序号)。
| A.氢气还原氧化铜实验中,先加热氧化铜后通氢气 |
| B.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拨开橡皮塞并投入碎瓷片 |
| C.实验室做钠的实验时,余下的钠屑投入到废液缸中 |
| D.配制浓硫酸与酒精混合液时,将1体积的酒精倒入3体积的浓硫酸中 |
E.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
F.制乙烯时,用量程为300℃的温度计代替量程为200℃的温度计,测反应液的温度
(2)苯、四氯化碳、乙醇、汽油是常见的有机溶剂,能与水互溶的是;不溶于水,且密度比水小的是。
(3)一瓶无色气体,可能含有CH4和CH2==CH2,或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?,
。
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如右图所示。
(1)如果A是淡黄色固体,
①写出B、E的化学式:B 、E 。
②C→D的化学方程式为_____________________。
③将足量的物质C通过入BaCl2溶液中,下列说法正确的是___________(填字母序号)。
a.溶液没有明显变化
b.溶液中出现白色浑浊
c.若继续通入Cl2或NH3,溶液都出现白色浑浊
(2)如果A是无色气体:
D→E的化学方程式为 ;
E→C的离子方程式为 。
现有6种短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| W |
周期表中原子半径最小的元素 |
| U |
地壳中含量最多的金属元素 |
| R |
单质为空气的主要成分 |
| T |
M层上有6个电子 |
| X |
最外层电子数是次外层电子数的2倍 |
| Y |
氢化物水溶液呈碱性 |
| Z |
元素最高正价是+7价 |
完成下列空白(涉及W、U、R、T、X、Y、Z时,用元素符号表示):
(1)元素T的原子共有个电子;元素X的一种核素可测定文物年代,这种核素的
符号是。
(2)用电子式表示:
①气态化合物XR2_________________;
②元素W、R形成的10电子分子的形成过程______________________________。
(3)用离子方程式表示:
①元素Y与元素W形成的离子YW4+与NaOH溶液共热的反应 _____;
②元素U的单质与NaOH溶液反应_______________________________________。
(4)元素Z与元素T相比,非金属性较强的是,下列表述中能证明这一事实的
是(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。在T、X、Y、Z四种元素的最高价
氧化物的水化物中,化学性质明显不同于其他三种的是(用分子式表示),
理由是。
将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题: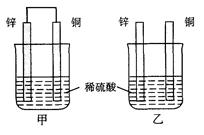
(1)下列说法正确的是____________。
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液的pH均增大 |
(2)在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为_______________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至
1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫
酸的物质的量浓度为_________________。