下列关于热化学反应的描述中正确的是( )
| A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热 ΔH=2×(-57.3) kJ·mol-1 |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+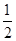 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
| C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g)ΔH=+571.6 kJ·mol-1 |
D.葡萄糖的燃烧热是2800 kJ·mol-1,则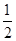 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1 |
在过氧化钾与水的反应中,其还原产物和氧化产物质量比为( )
| A.7∶4 | B.4∶7 |
| C.7∶2 | D.2∶7 |
Li不可能具有的性质是( )
| A.Li在空气中燃烧可生成Li2O2 |
| B.金属Li比金属铯的熔点高 |
| C.金属Li很软,用小刀可以切割 |
| D.金属Li可以保存在煤油中 |
钾的金属活动性比钠强,根本原因是()
| A.钾的密度比钠的小 |
| B.钾原子的电子层比钠原子多一层 |
| C.钾与水反应比钠与水反应更剧烈 |
| D.加热时,钾比钠更易汽化 |
将钠、钾分别投入相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为()
A.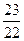 ∶ ∶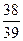 |
B.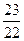 ∶ ∶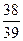 |
C.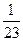 ∶ ∶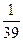 |
D.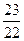 ∶ ∶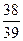 |
下列说法中符合碱金属特点的是()
| A.碱金属的盐都有焰色反应,而其单质及其氧化物则没有 |
| B.碱金属的单质及合金在通常情况下都是固体 |
| C.碱金属氧化物都是碱性氧化物,都易溶于水 |
| D.碱金属的绝大部分盐都是易溶于水的 |