下列相关反应的离子方程式书写错误的是
| A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO—+4OH—+2Fe(OH)3=3Cl—+5H2O+2FeO42— |
| B.少量SO2通入苯酚钠溶液中:2C6H5O—+SO2+H2O=2C6H5OH+SO32— |
| C.0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合: NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O |
| D.少量SO2通入NaClO溶液中:SO2 + ClO—+ OH—= SO42— + Cl— + H+ |
下列有关实验操作正确的是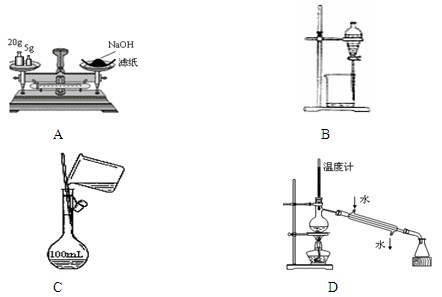
| A.称量氢氧化钠固体 | B.分离四氯化碳和水 |
| C.配制150 mL 0.10 mol·L-1盐酸 | D.分离两种沸点相差较大的液体互溶混合物 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| B.18克水所含的电子数为NA |
| C.8克氦气所含分子数为NA |
| D.3.2克氧气所含氧原子数为0.2NA |
实验室里需用490mL 0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是
| A.称取7.84g硫酸铜配成500mL溶液 | B.称取12.25g胆矾配成500mL溶液 |
| C.称取12.5g胆矾配成500mL溶液 | D.称取8.0g硫酸铜,加入500mL水 |
据科学家预测,月球的土壤中吸附着数百万吨的3He,每百吨3He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以4He的形式存在。下列说法中正确的是
| A.4He原子核内含有4个质子 | B.3He和4He互为同位素 |
| C.3He原子核内含有3个中子 | D.4He的最外层电子数为2,故 4He具有较强的金属性 |
已知最外层电子数相等的元素原子具有相似的化学性质。硫元素原子的核外电子分层排布示意图为,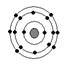 下列原子中,与硫元素原子化学性质相似的是
下列原子中,与硫元素原子化学性质相似的是
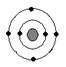
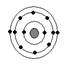

氖碳镁氧
A B C D