以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 |
过氧化氢溶液浓度/% |
过氧化氢溶液质量/g |
温度/℃ |
二氧化锰用量/g |
氧气体积/ml |
反应所需时间/s |
| ① |
5 |
12 |
20 |
0.2 |
125 |
11 |
| ② |
30 |
12 |
20 |
0.2 |
125 |
2 |
| ③ |
30 |
12 |
40 |
/ |
125 |
148 |
| ④ |
30 |
12 |
90 |
/ |
125 |
82 |
(1)通过实验①和②对比可知,化学反应快慢与 有关;
(2)通过对比实验 和 可知,化学反应快慢与温度的关系是 。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是 。
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应。
(1)实验准备
①查阅资料:NaHCO3+NaOH=====Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考。
| NaHCO3溶液 |
NaOH溶液 |
Na2CO3溶液 |
|
| 加入稀盐酸 |
现象Ⅰ |
无明显变化 |
产生气泡 |
| 加入澄清石灰水 |
溶液变浑浊 |
无明显变化 |
现象Ⅱ |
| 加入CaCl2溶液 |
无明显变化 |
溶液变浑浊 |
溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 |
澄清石灰水 变浑浊 |
澄清石灰水 无明显变化 |
澄清石灰水 无明显变化 |
表中的现象Ⅱ为_________
(2)实验过程
【实验1】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是__________。
有同学提出这个实验不足以证明有Na2CO3生成,其理由是_________。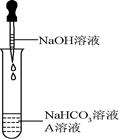
【实验2】证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是________。
某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红是因为碱在水溶液中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?为此他们设计了如下图所示的3个实验,请你和他们一起探究。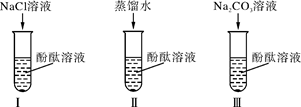
(1)实验Ⅰ可以证明____________________________________。
(2)实验Ⅱ加入蒸馏水的目的是____________________________;小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是______________________________________。
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到_____________________________________。
由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞溶液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-”。你认为Na2CO3溶液中存在OH-的原因是______________________________________。
化学教材 “寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】(1)氧化铁能否作过氧化氢溶液分解的催化剂?
(2)氧化铁与二氧化锰催化效果哪个好?
【实验探究】
| 实验步骤 |
实验现象 |
| ①分别量取5 mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 |
A试管中产生大量气泡,带火星木条复燃,B试管中的现象 |
| ②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象。 |
试管中均产生大量气泡,带火星木条均复燃 |
| ③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g。 |
|
| ④分别量取5 mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入a g氧化铁粉末,向D试管中加入a g二氧化锰粉末,观察现象。 |
  |
(1)A中产生的气体是 ;B试管中的现象。
(2)实验②、③证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式 。
(4)实验设计④的目的是,若实验④观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
小明家的新房装修,瓦工师傅用石灰浆(主要成分是氢氧化钙)抹墙。收工时瓦工师傅把未用完的石灰浆用沙土盖上,以备第二天再用,这样做的目的是防止石灰浆因变质而失效。
(1)请你根据所学知识写出石灰浆变质的化学方程式。
(2)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验。
| 实验步骤 |
实验现象 |
实验结论 |
|
| 取样,加一定量的水充分溶解后,过滤。 |
取少量滤渣于试管中,加入足量。 |
反应的化学方程式为 ; 实验的结论是该石灰浆部分变质。 |
|
| 取少量滤液于试管中,滴入无色酚酞试液。 |
(3)由此小明联想到实验室里的一些药品必须密封保存。实验室中必须密封保存的药品可分为以下几类:
①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如;
③,如浓硫酸。
某学习小组做镁带在空气中燃烧实验时,发现生成物中有黑色固体。针对这一现象,他们开展了如下探究活动。请仔细阅读并完成下列探究报告。
【探究目的】探究镁在空气中燃烧产生的黑色固体是镁与空气中什么物质反应产生的。
【分析猜想】分析空气中各种成分,寻找猜想依据。
空气成分之一:,化学性质稳定,一般不与其他物质反应。
空气成分分之二:氧气,氧气与镁反应生成的氧化镁是白色固体。
空气成分之三:水蒸气,打磨光亮的镁带放入沸水中,表面会附有白色固体并产生大量气泡;再向沸水中滴入无色酚酞试液,呈现红色,如果将镁带放到水蒸气中,也会发生上述反应,但产生的不是黑色固体。
空气成分之四:氮气、二氧化碳。猜想:可能是镁与N2或CO2反应生成黑色固体。
【实验一】镁带与氮气的反应
获取氮气
(1)把空气液化,然后蒸发,先蒸发出来的气体就是氮气,这种方法属于变化,但在实验室里空气不易被液化。
(2)以下是获取氮气的方法及装置(装置中使用的固体药品均过量),其中得到氮气较纯的是。(填字母)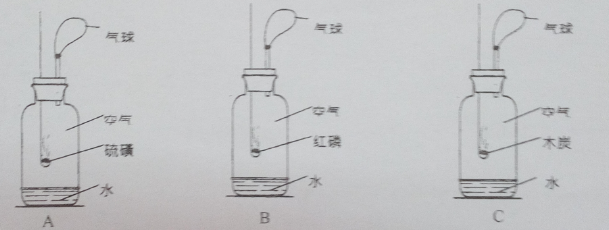
二、燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,配内壁附着一层淡黄色的固体。
三、实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁(Mg3N2)。该反应的化学符号表达式是。
【实验二】将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内出现白色固体和黑色固体。CO2与镁发生反应,根据所学知识猜想生成的黑色固体物质是。
【探究结论】镁在空气中燃烧产生的黑色固体是镁与空气中CO2反应产生的。