某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaHCO3、NaCl中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温、同压下测定)有剩余气体。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是
①粉末中一定有Na2O、Na2O2、NaHCO3
②粉末中一定不含有Na2CO3和NaCl
③粉末中一定不含有Na2O和NaCl
④无法肯定粉末中是否含有Na2CO3和NaCl
| A.①② | B.②③ | C.③④ | D.①④ |
氢化钙(CaH2)可作为生氢剂,反应的化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑,下列说法不正确的是
| A.CaH2既是还原剂,又是氧化剂 | B.H2既是氧化产物,又是还原产物 |
| C.CaH2是还原剂,H2O是氧化剂 | D.氧化产物与还原产物质量比为1∶1 |
下列变化的实质相似的是
①浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
②二氧化硫和氯气均能使品红溶液褪色
③二氧化硫能使品红溶液、溴水褪色
④氨气和碘化氢气体均不能用浓硫酸干燥
⑤常温下浓硫酸用铁制容器存放、加热条件下浓硫酸能与木炭反应
⑥浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
⑦二氧化碳、二氧化硫使澄清石灰水变浑浊
| A.只有②③④ | B.只有⑤⑦ | C.只有③④⑥⑦ | D.全部 |
下列混合物的分离或提纯操作中不正确的是
| A.除去N2中的少量O2,可通过灼热的Cu网后,收集气体 |
| B.除去Fe(OH)3胶体中混有的Cl- 离子,可用渗析的方法 |
| C.除去乙醇中的少量NaCl,可用蒸馏的方法 |
| D.重结晶、滴定操作都可用于提纯物质 |
SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
下列有关说法错误的是
| A.氧化性:Cr2O72->Fe3+>SO2 |
| B.K2Cr2O7能将Na2SO3氧化成Na2SO4 |
| C.每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA |
| D.若有6.72 L SO2(标准状况)参加反应,则最终消耗0.2 mol K2Cr2O7 |
下列有关实验装置进行的相应实验,能达到实验目的的是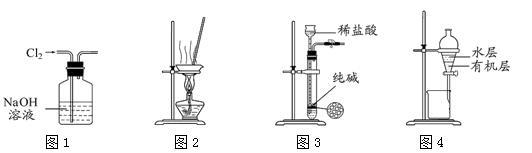
| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3所示装置制取少量纯净的CO2气体 |
| D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |