下列依据热化学方程式得出的结论正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.已知C(s)+O2(g)=CO2(g) ΔH1 C(s)+1/2O2(g)=CO(g);ΔH2,则ΔH2>ΔH1 |
| C.已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol,则含20 g NaOH的稀溶液与稀盐酸完全中和,中和热为28.65 kJ/mol |
对于m A (g)+n B (g) p C(g)+q D(g)的平衡体系,当升高温度时,平衡混合气体对氢气的相对密度从16.5变成16.9,则下列说法正确的是 ( )
p C(g)+q D(g)的平衡体系,当升高温度时,平衡混合气体对氢气的相对密度从16.5变成16.9,则下列说法正确的是 ( )
| A.m+n> p+q,正反应是放热反应 |
| B.m+n> p+q,正反应是吸热反应 |
| C.m+n< p+q,逆反应是放热反应 |
| D.m+n< p+q,逆反应是吸热反应 |
有一处平衡状态的反应X(s)+3Y(g) 2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是()
2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是()
①升高温度;②降低温度;③增大压强;④减小压强;⑤加入催化剂;⑥及时分离出Z。
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |
相同容积的四个密闭容器中进行同样的可逆反应:
2A(g)+B(g)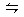 3C(g)+2D(g)
3C(g)+2D(g)
起始时四个容器所盛A、B的物质的量分别为
| 甲 |
乙 |
丙 |
丁 |
|
| A/mol |
2 |
1 |
2 |
1 |
| B/mol |
1 |
1 |
2 |
2 |
在相同温度下建立平衡时,A或B的转化率大小关系正确的是()。
A.αA:甲<丙<乙<丁 B.αA:甲<乙<丙<丁
C.αB:甲<丙<乙<丁 D.αB:丁<乙<丙<甲
在某固定容积的密闭容器中存在化学平衡:a A(g) b B(g)+c C(g),在温度不变的条件下,再充入一定量的A 物质,重新达到平衡时,下列判断中正确的是()
b B(g)+c C(g),在温度不变的条件下,再充入一定量的A 物质,重新达到平衡时,下列判断中正确的是()
| A.若a=b+c时,B的物质的量分数变大 |
| B.若a=b+c时,B的物质的量分数不变 |
| C.若a>b+c时,A的转化率不变 |
| D.若a<b+c时,A的转化率变小 |
一定温度下,在一定容的密闭容器中充入N2和H2发生如下反应:N2+3H2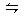 2NH3,并达到平衡,此时N2的转化率为a%,缩小容器的体积,则N2的转化率将()
2NH3,并达到平衡,此时N2的转化率为a%,缩小容器的体积,则N2的转化率将()
| A.增大 | B.减小 | C.不变 | D.无法确定 |