下面各装置图能达到实验目的的是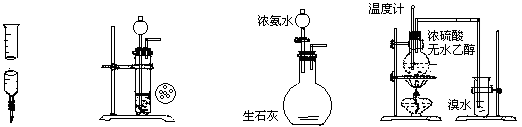
Ⅰ Ⅱ Ⅲ Ⅳ
| A.实验Ⅰ量取20.0mL的H2SO4待测液放入锥形瓶中 |
| B.实验Ⅱ用CaC2和饱和食盐水反应制取C2H2 |
| C.实验Ⅲ制取氨气 |
| D.实验Ⅳ溴水褪色证明了乙烯可以与溴发生加成反应 |
用滴有酚酞和氯化钠试液的湿润滤纸分别做甲、乙两个实验,能发现附近变成红色的电极是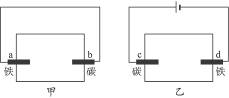
| A.ac | B.bd | C.ad | D.bc |
下图X、Y分别是直流电源的两极,通电后发现a极板质量增加,d极板有无色无臭气体放出,符合这一情况的是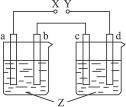
| A极板 |
d极板 |
X电极 |
Z溶液 |
|
| A |
锌 |
石墨 |
负极 |
CuSO4 |
| B |
石墨 |
石墨 |
负极 |
NaOH |
| C |
银 |
铁 |
正极 |
AgNO3 |
| D |
铜 |
石墨 |
负极 |
CuCl2 |
用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解溶液的pH下降的是
| A.CuCl2 | B.AgNO3 | C.BaCl2 | D.H2SO4 |
电解水时为了增强其导电性不应加入的电解质是
| A.NaOH | B.CuSO4 | C.H2SO4 | D.KNO3 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)====Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-="===" Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |