下列变化中所涉及到的物质都是初中化学常见的物质,已知A、B常温下为液态,C、G为单质,医疗上用F来配制生理盐水.试回答下列问题:
①A在一定条件下反应生成B和C;
②D与E反应生成F和B;
③C与G在不同条件下反应生成H或I;
④J和K分别与D反应都生成B、F和I,J中的组成元素比K多一种.
(1)写出E的化学式 .
(2)D所属物质类别 (填“酸、碱、盐或氧化物”);
(3)写出A在一定条件下生成B和C的化学反应方程式 ;
(4)④中的变化涉及到的基本反应类型有 .
(5)将等质量的J和K分别加入到足量的D溶液(质量分数都相同)中,比较反应产生I快慢,并说明理由
.
现有①洁净的空气 ②铁粉 ③高锰酸钾 ④冰水共存物 ⑤湖水 ⑥氧化铁 ⑦高锰酸钾制氧气后的固体剩余物 ⑧液氧 ⑨5%的过氧化氢溶液 ⑩水银十种物质,其中属于混合物(填序号,下同) ,属于单质的有 ,属于氧化物的有 。
用数字和化学符号表示:
(1)2个亚铁离子_______________;(2)3个铵根离子_______________;
(3)保持氮气化学性质的最小微粒_______________;
(4)碳酸钠中碳元素的化合价为+4价____________;
(5)铯(Cs)原子的结构示意图为 ,铯原子在化学反应中易形成铯离子_______________;
,铯原子在化学反应中易形成铯离子_______________;
(6)+6价硫元素的氧化物的化学式 SO3;
某兴趣小组利用氨水能使酚酞试液变红的原理,设计如下实验以探究微粒的运动。请回答实验中的有关问题。(1)实验I:在盛有少量蒸馏水的小烧杯中滴入2滴~3滴酚酞试液,再向其中滴加浓氨水。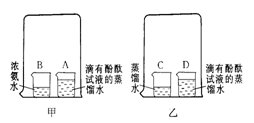
由实验I得出的结论有
(2)实验Ⅱ(如甲图):烧杯A中的现象是_________ ;产生的原因是_________________ 。
(3)为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如图乙)作为对比实验。你认为有无必要,理由是______________________ 。
(8)化学实验基本操作在化学学习和研究中具有重要作用。现有:
a试管、b漏斗、c酒精灯、d集气瓶、e广口瓶、f胶头滴管、g量筒(10mL,50mL,100mL)、h药匙、i石棉网、j试管刷等仪器,请为下列实验操作各选一种。(用序号填空)
(1)用于作热源的仪器是 ;(2)吸取或滴加少量液体使用 。
(3)可以直接在酒精灯火焰上加热的玻璃仪器是 (4)用于洗涤仪器内壁的工具是 ;
(5)贮存固体药品的仪器是 ;(6)加热时常垫在玻璃容器与热源之间的用品是 。
(7)取用粉末状固体药品用到的仪器是 ;
(每空1分共7分)(1)用符号表示:
①铝原子___________②三个钠离子___________③4个氮原子___________④氯离子___________
(2)我们生活在物质世界中,每天都要接触很多物质:如①海水 ②氯化钠 ③铜 ④自来水 ⑤空气 ⑥牛奶 ⑦食醋 ⑧氧气 ⑨氧化铜 ⑩氮气,属于混合物的有(填序号)__ __
(3)试用分子和原子的观点解释下列问题
①氧气和氢气都是由分子构成的,但它们的化学性质却不相同。
②酒精挥发和酒精燃烧的本质微观区别。