学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液.小红同学想探究废液中溶质的成分,请你一同探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【做出猜想】小红认为废液中的溶质只有CaCl2.你认为还可能含有的溶质是 .(化学式)
【查阅资料】CaCl2溶质呈中性.
【实验与结论】为了验证小红的结论,小红进行了下面是的实验:
| 实验操作 |
实验现象 |
结论 |
| 取少量废液于试管中,向其中滴加几滴无色酚酞溶液 |
溶液呈 . |
废液中只有 ,自己的猜想正确 |
(1)你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 .
(2)如果想要证明我的猜想是正确的,请补充完下面的实验方案
| 实验操作 |
实验现象 |
| ①取少量废液与试管中,向其中加入石蕊溶液 |
废液变为 |
| ②取少量废液与试管中,向其中加入 . |
有气体产生 |
| ③取少量废液与试管中,向其中加入 . |
(3)若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完成过 .
(8分)某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验。
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。
请你对脱脂棉燃烧的原因进行分析_______。
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了。
【提出问题】溶液为什么先变红,过了一会,红色又褪去了呢?
【猜想】甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故。乙同学认为甲同学的猜想不正确,理由是_____________________。
【查阅资料】①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色。
【猜想】通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原凶义进行了猜想。
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓。
【实验探究】请你将下列实验方案填写完整。
| 猜想 |
实验操作 |
实验现象 |
结论 |
| A |
取过氧化钠与水反应后的溶液放入试管中,_____ ___________________________________________ |
_________________ |
猜想A 正确 |
| B |
取过氧化钠与水反应后的溶液放入试管中, ________________________________________ |
________________ |
猜想B 错误 |
【得出结论】根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,则另一反应的化学方程式为____________________________________。
(12分)化学实验是学习化学的基础,请根据下列装置图回答问题。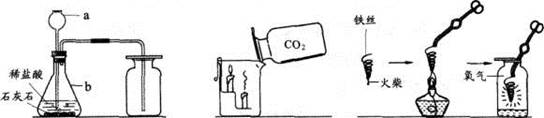
A B C
(1)写出仪器a、b的名称_______;b_______。
(2)写出A图中产生气体的化学方程式____________________________。
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有_______、_______和_______性质。这一性质在实际生活中的应用为_______。
(4)C图中螺旋状铁丝的末端系一根火柴的作用是_______。
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是_______。
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。请你分析回答:
| 物质 |
镁条 |
含碳0.05%的铁丝 |
含碳0.2%的铁丝 |
含碳0.6%的铁丝 |
| 燃烧时 的现象 |
剧烈燃烧,发出 耀眼白光,无火星 |
剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
(未填) |
金属钠很软,可以用刀切割。切开外皮后,可以看到钠具有银白色的金属光泽。钠是热和电的良导体。钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃。将金属钠放入水中,可以反应生成NaOH和H2;钠跟氧气混合加热生成淡黄色的过氧化钠(Na2O2)固体,钠跟CO2在加热条件下反应生成碳酸钠和单质碳。
(1)试写出钠跟水反应的化学方程式
(2)小刘同学用图A装置做钠跟氧气反应实验,观察到生成物中出现黑色固体,则该黑色固体是(填化学式),试写出相应的化学反应方程式
_________________________________。
(3)为了探究黑色固体成分,小刘同学进行了下列探究。探究反应中CO2的
猜想①:CO2的来源于 ;猜想②:CO2的来源于 ;
在上述两种来源中,(填序号)是CO2的主要来源。用图B和C装置实验的目的是 。
下列A ~ F是初中化学中的六个实验,请按要求填空:
(1)D实验中烧杯③的作用是,F实验中搅拌的目的是。
(2)B实验中红磷燃烧的化学方程式为,实验说明氧气的体积约占空气的,实验成功的关键是(填序号)。
①装置气密性好;②实验前夹紧止水夹;③红磷过量或足量;④冷却后再打开止水夹;⑤要选用教室内的空气。
(3)E实验的全过程观察到的现象是
;发生反应化学方程式为。
(4)上述实验中能达到实验目的且正确的是(填字母)。
三聚氰胺(化学式为C3H6N6)是一种白色结晶粉末,无气味,低毒,对人体有着某种危害作用,在有机化工中用途广泛;因其含氮量高,而俗称“蛋白精”。2008年卫生部查明,不法分子为了提高婴幼儿奶粉中的蛋白质含量而加入三聚氰胺,导致发生多起婴幼儿泌尿系统结石病例,在社会上引起了广泛关注。某化学兴趣小组的同学欲探究三聚氰胺的制取原理:
【查阅资料】
(1)目前,化工企业常用尿素合成法制取三聚氰胺。即以尿素[化学式:CO(NH2)2]为反应物,硅胶为催化剂,在380℃至400℃的温度下,沸腾反应、冷凝得到三聚氰胺,同时产生两种无色气体,其中一种气体具有刺激性气味。
(2)NO是无色气体,不溶于水,在空气中能迅速氧化为红色NO2气体。
【提出问题】
反应生成的两种气体是什么?
【假设猜想】
根据资料及反应物质判断,生成的两种气体可能是:
①二氧化碳和水蒸气;②二氧化碳和氨气;
③二氧化碳和氮气;④二氧化碳和二氧化氮;
• • • • • •
提出以上猜想的依据是 ;
你认为合理的猜想是(填序号 ,理由是
【设计实验】
同学们在老师的指导下,设计下图所示实验摸拟制取三聚氰胺,并验证猜想。
A装置的作用是使生成的三聚氰胺迅速凝华而与气体分离。
【实验现象和分析】
(1)实验观察到B中棉花变红,则证明生成了 ,同时看到D中________________现象,说明还生成了二氧化碳。
(2)C中浓硫酸的作用是 。
【实验结论】
根据资料和实验现象分析可知,用尿素分解制取三聚氰胺的化学方程式为
___________________________________________________________。