某化学活动小组开展了一次关于金属镉与铜、银活动性顺序的探究.
[提出问题]这三种金属活动性顺序是怎样的?
[猜想假设]猜想①:Cu>Cr>Ag 猜想②:Cu>Ag>Cr 猜想③:
[查阅资料]
①镉(Cr)是一种银白色金属,在化合价中通常表现为+2价.
②水体中镉元素通常以氯化镉的形式存在.
③氯化镉、硝酸镉都能溶于水,氢氧化镉难溶于水.
[实验探究]
| 实验步骤 |
实验现象 |
实验结论 |
化学方程式 |
| 取适量镉、铜、银与试管中,加入适量 稀盐酸(或稀硫酸) |
镉表面有气泡产生,铜银表面无气泡产生 |
|
写出镉和稀盐酸反应的化学方程式 |
| 取适量铜片与试管中,加入少量的硝酸银溶液 |
, |
铜的活动性顺序大于银 |
铜与硝酸银反应的化学方程式 |
[实验结论]活动性由强到弱的顺序:
[反思]实验中需对金属片用砂纸打磨,其目的是 .
(7分)实验室制取气体的装置如图所示,根据所学的知识回答下列问题。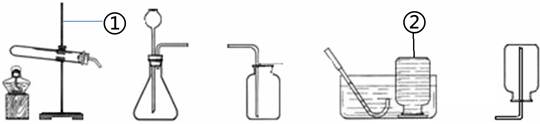
A B C DE
(1)图中标有①、②的仪器名称:① ;② 。
(2)写出用A或B制取氧气的一个化学方程式,可选用图中和(填标号)组装一套制取较纯氧气的装置,判断氧气集满的方法是。
化学兴趣小组用下图装置进行实验,发现镁片完全溶解、石灰水浑浊。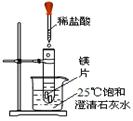
(一)石灰水变浑浊的原因是:
(1)镁和盐酸的反应(填“吸热”或“放热”)。
(2)。
(二)甲同学测得反应后试管内溶液pH<7
(1)该溶液呈(填“酸”、“碱”或“中”)性。
(2)该溶液pH<7的可能原因是:
①MgCl2溶液的pH<7; ②。
(三)乙同学将反应后试管内溶液冷却,加入镁粉并滴入酚酞,溶液颜色无变化,再加热,发现溶液慢慢浑浊且变红。
【猜想】对实验中“溶液慢慢浑浊且变红”的原因,乙同学提出猜想:
MgCl2+2H2O=Mg(OH)2↓+2HCl大家都认为此猜想不合理,理由是。
【查阅】资料1:Mg(OH)2难溶解于水,升高温度可加大其在水中的溶解度。
资料2:K、Ca、Na、Mg等活泼金属在一定条件下能与水反应,产生碱和气体。
【实验】丙同学在滴有酚酞的热水中加入镁粉,观察到液体慢慢变红并浑浊,镁粉表面产生气泡。收集并点燃气体,发现能燃烧,该气体是。
用化学方程式表示:乙同学实验中“溶液慢慢浑浊且变红”的原因。
(9分)下图为实验室常用的实验装置。回答问题: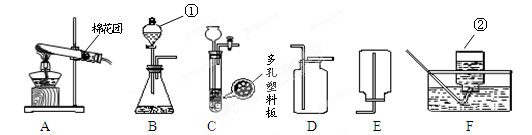
(1)标号仪器的名称:①;②。
(2)A、F组合制氧气,氧气收集完毕,应先(填“熄灭酒精灯”或“从水中取出导气管”)。
(3)用B、D组合制取气体的化学反应方程式。
若将发生装置由B改为C,其优点是。
(4)硫化氢气体(H2S)有毒,溶于水形成酸。用块状硫化亚铁(FeS)和稀硫酸发生复分解
反应制得H2S,反应化学方程式为。某同学用下图G、H 、I组合收集H2S。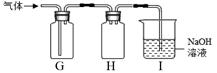
①G收集H2S,说明其密度比空气(填“大”或“小”)。
②各装置的作用:H、I。
某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如图1的实验装置。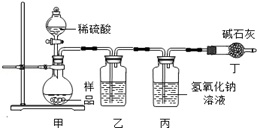
图1
①实验装置乙中盛放的试剂为 ,
其作用是;
装置丁中碱石灰的作用是 。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
质量分数 (填写“偏高”“偏低”或“不变”).
③小明同学认为小科的方案存在问题,即使操作规范下也会造成结果偏低,你
认为他的理由是,应该将装置甲中双孔橡
胶塞换成三孔橡胶塞,并增加图2装置,实验结束后缓缓通入一段时间空气,
目的是,其中NaOH溶液的作用是 。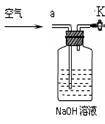
图2
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即Na2CO3已完全反应)的方法是: 静置,向上层清液中滴加溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、操作X、干燥、称量沉淀的质量为10.0g,操作X的名称是,如果缺少此操作会造成碳酸钠质量分数(填写“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为 。(写出计算过程,结果保留至0.1%,共3分)
根据下列实验装置图填空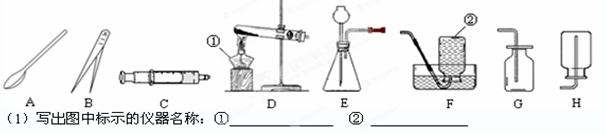
(2)实验室用KMnO4制取较纯净的O2,应选用的发生装置为(填字母序号,下同),收集装置为,取用KMnO4药品时,应选用仪器把药品小心地送至试管底部,写出该反应的化学方程式。
(3)组装发生装置D时,下列仪器用品的组装正确顺序是:铁架台 → 木块 → → 。
①试管②酒精灯 (填写序号,此小题共1分)
(4)注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至处。
②将注射器C连接到装置E的导管口处,向前推进注射器活塞,若看见(填字母)时,则说明E装置气密性良好。
A.长颈漏斗口有气泡冒出 B.锥形瓶中液面上升 C.长颈漏斗中液面上升,并形成稳定水柱
(5)常温下,硫化氢是一种有臭鸡蛋气味的气体,能溶于水,密度大于空气,实验室通常在常温下用硫化亚铁固体(FeS)和稀硫酸反应制得,同时生成硫酸亚铁,则从上面装置中选择的发生和收集装置组合为_______,化学反应方程式 。
(6)在实验室中,I装置被称做“万能瓶”,具有多种用途,仔细观察装置的特点回答下列问题: 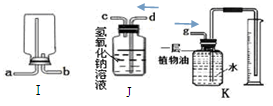
①实验室收集气体若用I装置替代G装置,
则气体应从口进入(填a或b)。
②从J、K装置中任选一个,阐述该装置的
用途:。