依据事实,写出下列反应的热化学反应方程式。
(1)在25℃、101kPa下,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为 _________________________________________________。
(4)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 。
(1)写出下列反应的化学方程式:
①铝热反应(铝粉与四氧化三铁):;
②铜片与过量的浓硫酸共热:;
(2)写出下列反应的离子方程式:
③铵盐溶液与烧碱溶液共热:;
④铜片与浓硝酸反应:。
降低大气中CO2的含量、减缓温室效十分重要。
(1)工业上有一种方法是用CO2来生产甲醇:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 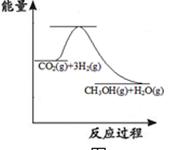
上图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。该反应是(填“吸热”或“放热”)反应。
(2)某温度下,若将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如下图实线所示。则加入催化剂的曲线是(填:a或b);
0—8min内该反应的平均速率v(CO2)=mol/(L·min)。
(3)在CO跟O2的反应中,破坏1molCO中的化学键消耗的能量为a kJ,破坏1molO=O键消耗的能量为bkJ,形成1molC=O键释放的能量为ckJ。则1molCO在空气中完全燃烧生成CO2放出的能量为
kJ。
只用一种试剂来鉴别下列各组物质:
(1)甲醇、乙醛、乙酸,选用的试剂是。
(2)乙酸、甲酸甲酯、乙酸乙酯,选用的试剂是。
(3)苯、四氯化碳、1—已烯、苯酚的水溶液,选用的试剂是。
丙烯可用于合成是杀除根瘤线虫的农药B(分子式为C3H5Br2Cl),该分子中每个碳原子上均连有卤原子,其合成路线如下图所示。
(1)丙烯的结构简式是 ,它含有的官能团名称是。
,它含有的官能团名称是。
(2) 由A生成B的反应类型是。
由A生成B的反应类型是。 (3)A水解可得到 CH2=CHCH2OH,该水解反应的化学方程式为:。
(3)A水解可得到 CH2=CHCH2OH,该水解反应的化学方程式为:。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X极附近观察到的现象是。
②Y电极上的电极反应式是;把湿润的碘
化钾淀粉试纸放在Y电极附近,现象是。
(2)要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:X电极的材料是,
Y电极上发生的电极反应式为。(说明:杂质发生的电极反应不必写出)