溴及其化合物广泛应用在有机合成、化学分析等领域。
(1)海水提溴过程中溴元素的变化如下: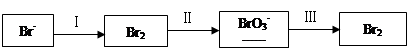
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。
ⅰ.通入氯气后,反应的离子方程式是______。
ⅱ.调海水pH可提高Cl2的利用率,用平衡原理解释其原因是______。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
Br2+ Na2CO3=
Na2CO3= NaBrO3+
NaBrO3+ CO2+
CO2+ ______
______
③过程Ⅲ,用硫酸酸化可得Br2和Na2SO4的混合溶液。
相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是______。
(2)NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
| 粒子 |
I2 |
Br2 |
IO3- |
| 物质的量/mol |
0.5 |
1.3 |
|
则原溶液中NaI的物质的量为______mol。
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0% .
(1)X的电子式是;
(2)X与金属钠反应放出氢气,反应的化学方程式是(有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是;Y能发生银镜反应,Y与银氨溶液的反应的化学方程式是:。
工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。路线①②③是工业生产硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
(1)写出N2的一种用途。
(2)实验室制取物质NH3的化学方程式为。
(3)写出工业制硝酸第③步反应化学方程式。
(4)硝酸是一种强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。 实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(ⅰ)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:___________。该反应中发生氧化反应的物质是_______,1 mol氧化剂_________(填“得到”或“失去”)_______ mol电子。
(ⅱ)48.0 g Cu与适量的浓HNO3反应,铜全部溶解后,共收集到标准状况下22.4 L的气体(NO2和NO的混合气体),反应中消耗HNO3的物质的量是()
| A.1.5 mol | B.2.0 mol | C.2.5 mol | D.3.0 mol |
(ⅲ)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等。请将3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
HNO3+ ______  ______+ ______ + N2O↑ + H2O
______+ ______ + N2O↑ + H2O
并配平其对应的离子方程式:□Fe2++□NO3-+□H+ =□Fe3++□N2O↑+□H2O
原子序数依次增大的A、B、C、D都是元素周期表中短周期元素,B、C、D同周期,A、D同主族,且A的原子结构中最外层电子数是电子层数的3倍。D的最高价氧化物对应的水化物为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。根据以上信息,回答下列问题:
(1)D元素在元素周期表中的位置为,A和B形成化合物的化学式是。
(2)高温时,C的单质跟Fe2O3发生反应的化学方程式。
(3)写出C的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物反应的离子方程式。
下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
④ |
⑤ |
⑥ |
⑧ |
⑩ |
|||
| 3 |
① |
⑦ |
⑨ |
|||||
| 4 |
② |
③ |
(1)在这10种元素中,化学性质最不活泼的是(写序号),失电子能力最强的原子是_____(用元素符号表示)。
(2)在这10种元素中,最高价氧化物的水化物碱性最强的是(填化学式),最高价氧化物的水化物酸性最强的是(填化学式)。
(3)H分别与④、⑤、⑦、⑧、⑨形成的化合物中,最稳定的是(填化学式);
(4)①、⑧、⑨三种元素单核离子半径由小到大的顺序是(用相应的离子符号表示):
(5)写出③和⑨形成的化合物的电子式,化学键类型为____(“离子键”或“共价键”)。
用化学方程式或离子方程式解释下列现象:
(1)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:请写出该原理的化学方程式______________
(2)Cl2通入FeCl2溶液中可将Fe2+氧化,请写出该反应的离子方程式:______________