以下是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。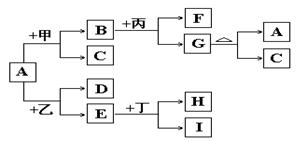
(1)若F是由Na+和SO42-组成的溶液,则甲的化学式是 ,列举A物质的一种用途 。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为 ,丁属于单质、酸、碱中的 ;在I溶液中加入氢氧化钠溶液,可以观察到的现象是 ,对应的离子方程式和化学方程式依次是 ,
;
(3)写出G A+C的化学方程式: 。
A+C的化学方程式: 。
(4)若A中混有杂质Al2O3,除去杂质的方法是加入过量的 ,该反应的离子方程式为 。
(5)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1。则反应物中Fe2O3、Fe、H2SO4的物质的量之比为____ ____。
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原
子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:。F的原子结构示意图为:。
(2)B、D形成的化合物BD2中存在的化学键为键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:。
(4)A、C、D、E的原子半径由大到小的顺序是(用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性于F(填“强”或“弱”),并用化学方程式证明上述结论。
已知X、Y是阳离子,Z是阴离子,M、N是分子,它们都由短周期元素组成,且具有
以下结构特征和性质:
①X、Y、M、N的核外电子总数相等;②常温下,M是极易溶于N的气体;③X与M均由相同的元素组成;④Y为单核离子,其与Z组成的物质可用于净水;⑤Z由同主族元素组成。请回答下列问题:
(1)X的电子式为,Z的离子符号为。
(2)X与Z形成的化合物中所含有的化学键类型为。
(3)写出Y与M、N形成的混合物发生反应的离子方程式:。
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列
问题: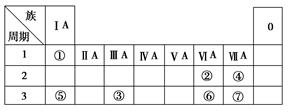
(1)④、⑤、⑦的原子半径由大到小的顺序为(用元素符号表示,下同)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为>。
(3)①、②两种元素按原子个数之比为1∶1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式。
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
①写出D溶液与G反应的化学方程式。
②写出检验A溶液中溶质的阴离子的方法:。
③常温下,若电解1 L 0.1 mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为mol。
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有。
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热
条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液洗后得到无色溶液F,溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。请回答下列问题:
(1)组成单质A的元素在周期表中的位置是。
(2)组成单质B的元素的原子结构示意图为。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯,该反应的氧化剂为。
(4)溶液F在空气中长期放置生成H的化学方程式为。
(5)H的溶液与稀硫酸反应产生的现象为。
下表是元素周期表主族元素的一部分,短周期元素X的最高正化合价是+5,Y的单质
可在空气中燃烧。
| W |
X |
Y |
| Z |
请回答下列问题:
(1)Z的元素符号是,写出Z的原子结构示意图:。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,该反应的离子方程式为。
(3)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中Z用元素符号表示)
| 编号 |
性质推测 |
化学方程式 |
| 示例 |
氧化性 |
H2ZO3+4HI=Z↓+2I2+3H2O |
| 1 |
||
| 2 |
(4)由C、O和Y三种元素组成的化合物COY中,所有原子的最外层都满足8电子结构。写出该化合物的电子式:。