为测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,称取一定质量的样品,甲同学利用图I所示装置测量产生CO2的体积,乙同学利用图II所示装置通过干燥管的增重测量产生CO2的质量,已知所用稀硫酸均足量。
(l)盛放稀硫酸的仪器名称为 ;
(2)试剂X为 ,试剂Y为 ;
(3)甲同学在进行实验时,为减小误差,应注意的事项有(填选项字母) ;
| A.读数前应使整套装置冷却至室温 |
| B.调整Z的高度使量气装置左右液面相平 |
| C.读数时视线与Z内凹液面最低点相切 |
| D.读数前应通入一定量的N2使生成的CO2全部进入量气装置 |
(4)按乙同学的实验方案进行实验,测得干燥管质量偏低的因素有 ,使测得的 Na2CO3的质量分数偏低的因素有(称量操作正确) (写一种)。
二茂铁(结构如图)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到。反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O
二茂铁的熔点为172~173℃,在100℃开始升华。能溶于乙醚、二甲亚砜等非极性溶剂,不溶于水,对碱和非氧化性酸稳定。制备的步骤如下:
步骤1.在150mL的三颈瓶中加入25g细粉末状KOH和60mL无水乙醚,通入氮气并搅拌约10分钟使之尽可能溶解,然后加入5.5 mL环戊二烯,再搅拌10分钟。
步骤2. 向烧杯中加入25 mL二甲亚砜和6.5g新制的无水氯化亚铁,微热至40℃并搅拌使其溶解,然后加入滴液漏斗中。
步骤3. 按图所示的装置装配好仪器,打开滴液漏斗的活塞,缓慢将氯化亚铁等加入三颈瓶中,并继续搅拌1小时。
步骤4. 反应结束后,将混合物倒入100mL 18%的盐酸溶液,将烧杯放在冰浴中冷却,搅拌约10分钟,使结晶完全。
步骤5. 抽滤,将获得的产品以冷水洗涤2~3次,低温风干得到粗制的二茂铁。
(1)步骤1中通入N2的目的可能是。
(2)步骤2中,滴液漏斗侧边的玻璃导管的作用是。
(3)实验装置中,冷凝管通水,水应从口进(选填a或b)。
(4)步骤4将反应后的混合物倒入盐酸中,发生主要反应的离子方程式是。
(5)步骤5用冷水洗涤是因为,因此可采用的方法,进一步提纯二茂铁。
Na2O2可用作漂白剂和呼吸面具中的供氧剂。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞试液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞试液变红是因为,红色褪去的可能原因是。
②加入MnO2反应的化学方程式为。
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
步骤1:按图示组装仪器(图中夹持仪器省略),检查气密性,装入药品;
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①盛装稀盐酸的仪器名称;B装置的作用是。
②必须检验氢气纯度的原因是。
③设置装置D的目的是。
④你得到的结论是(若能反应请用化学方程式表示)。
无水硫酸铜在强热下会发生分解反应:
CuSO4 CuO + SO3↑ 2SO3
CuO + SO3↑ 2SO3 2SO2↑+ O2↑
2SO2↑+ O2↑
用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1) 2SO3(g) 2SO2(g)+ O2(g)该反应的平衡常数表达式为K=。
2SO2(g)+ O2(g)该反应的平衡常数表达式为K=。
(2) B管中除温度明显升高外,还可看到的现象是,而温度明显升高的主要原因是;B管中发生反应的有关离子方程式是。
(3)仪器E的作用是。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为(用m表示)。
②如果不能,则原因是。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是。
NaClO2用于棉、麻、粘胶纤维及织物的漂白。实验室制备NaClO2的装置如下图所示: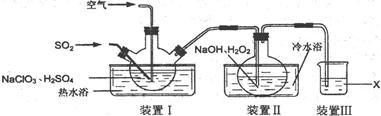
(1)装置I控制温度在35~55℃,通入SO2将NaClO3还原为ClO2(沸点:11℃),反应结束后通入适量的空气,其目的是。
(2)装置Ⅱ中反应生成NaClO2的化学方程式为。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是,检验该离子的方法是
(3)已知在NaClO2饱和溶液中温度低于38℃时析出晶体是NaClO2·3H2O,温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl。请补充从装置Ⅱ反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②;③;④;得到成品。
(4)装置Ⅲ中试剂X为。
一定量的浓硫酸与足量Zn充分反应时,有SO2和H2生成.某校化学研究性学习小组对此进行研究.按图组装好实验装置,微热试管A,观察到C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又会明显增加.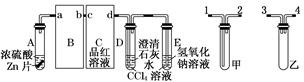
试回答:
(1)装置A中需用浓H2SO4,用一种简单的方法确定一瓶H2SO4一定是浓H2SO4:
________________________________________________________________________.
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接__________、________接b,c接________、____________接d;D、E两支试管中CCl4溶液的作用是_____________________________________________________________________.
(3)能证明浓硫酸具有强氧化性的实验现象为_____________________________;
反应较长时间后气泡量又会明显增加的原因是___________________________
(4)D中浑浊消失的离子方程式为____________________________________