制备锌印刷电路板是用稀硝酸腐蚀锌板,产生的废液称“烂板液”。“烂板液”中含硝酸锌外,还含有自来水带入的Cl—和Fe3+。在实验室里,用“烂板液”制取ZnSO4·7H2O的过程如下: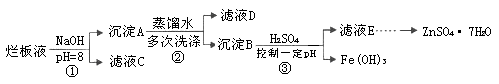
(1)若稀硝酸腐蚀锌板时还原产物为N2O,氧化剂与还原剂的物质的量之比是 。
(2)若步骤①的pH>12,则Zn(OH)2溶解生成四羟基合锌酸钠。写出Zn(OH)2被溶解的离子方程式 。
(3)滤液D中除了含有OH—离子外,还含有的阴离子有 (填离子符号)。
(4)若滤液E的pH=4,c(Zn2+)=2mol·L-1,c(Fe3+)=2.6×l0-9mol·L-1,能求得的溶度积是 (填选项)。
A.Ksp[Zn(OH)2] B.Ksp[Zn(OH)2]和Ksp[Fe(OH)3] C.Ksp[Fe(OH)3]
(5)步骤③要控制pH在一定范围。实验室用pH试纸测定溶液pH的方法是: 。
(6)已知:①Fe(OH)3(s) Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ•mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ•mol-1
②H2O(l)  H+(aq)+OH-(aq) ;ΔH=" b" kJ•mol-1
H+(aq)+OH-(aq) ;ΔH=" b" kJ•mol-1
请写出Fe3+发生水解反应的热化学方程式: 。
若①的溶度积常数为KSP,②的离子积常数为KW,Fe3+发生水解反应的平衡常数:
K= 。(用含KSP、KW的代数式表示)
化学与人的身心健康密切相关。
(1)当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题。请回答:
a、导致酸雨的主要气体是(填序号,下同)。① SO2② CO2
b、使臭氧层受到破坏的主要气体是。①二氧化碳②氟氯代烷
c、为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程式:
___。
(2)合理选择饮食,正确使用药物是保证身心健康的重要方面。请回答:在日常生活中,人们在选择食物时要考虑其酸碱性。下列食物中,属于酸性食物的是__(填序号)。
①猪肉②胡萝卜
金属是人类生产、生活中不可缺少的重要材料
(1)生铁是(填化学式)和铁的合金,生铁的硬度比纯铁(填高、低)。
(2)生铁放置在潮湿的空气发生电化学腐蚀时的正极反应为;负极反应为;用盐酸可以除去生铁表面的铁锈,该反应的离子方程式为。
(3)下列对金属制品采取的防护方法不正确的是(填序号)。
①在电线的外面包上一层塑料层
②在自行车钢圈上镀上一层金属铬
③在海轮的铁制外壳上焊上铜块
④在铁制的暖气片上刷一层油漆
(4分)有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱。请回答下列问题(填序号)。
(1) 由于具有兴奋作用,国际奥委会严禁运动员服用的药物是;
(2) 某同学胃酸过多,应选用的药物是;
(3) 从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是;
(4) 滥用药物会导致不良后果,如过量服用引起中毒,应立即停药,并静脉注射
NaHCO3的是。
下表是某品牌饼干包装上的部分说明。
| 品 名 |
××饼干 |
| 部分配料 |
①小麦粉 ② 白砂糖 ③ 食用棕榈油 ④ 鸡蛋 |
| 保质期 |
十二个月 |
| 生产日期 |
见封口 |
上表所列配料中,富含淀粉的是 (填序号,下同),富含油脂的是____,
富含蛋白质的是 ,属于调味剂的是。
(6分) 刻制印刷电路板得到的酸性废液中含有大量的FeCl2、CuCl2、FeCl3。为了减少污染并变废为宝,工程师们设计了如下流程,以常用的酸、碱和废铁屑为原料回收铜和制备铁红(Fe2O3)。
请回答
(1)原料③的焰色反应呈黄色,其化学式为____。
(2)加入原料①后发生的离子反应中,不属于置换反应的离子方程式为
____。
(3)若在实验室中完成操作②,其步骤包括搅拌和____,需要用到的玻璃仪器有
____(填字母)。
a.烧杯 b.漏斗 c.玻璃棒 d.酒精灯