根据下列实验内容得出的结论正确的是
| 选项 |
实验内容 |
结论 |
| A |
某气体的水溶液能使红色石蕊试纸变蓝 |
该气体一定是NH3 |
| B |
某气体能使紫色的酸性高锰酸钾溶液褪成无色 |
该气体一定是SO2 |
| C |
某物质的水溶液中加入盐酸产生能使澄清石灰水变浑浊的无色气体 |
该溶液一定含有CO32- |
| D |
某物质的水溶液中加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解 |
该溶液中至少含有SO42-、SO32-中的一种 |
下列各组性质比较中,正确的是
①酸性:HClO4>HBrO4>HIO4②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>Si>O④稳定性:HCl>H2S>SiH4
| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
下列各图中,表示正反应是吸热反应的图是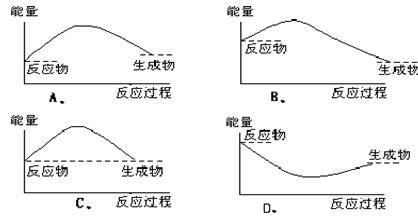
不久前,我国科学家在世界上首次合成3种新核素.其中一种新核素的名称是铪。关于铪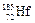 的说法正确的是
的说法正确的是
| A.发现了一种新的元素 | B.原子核内有185个质子 |
| C.原子核内有185个中子 | D.铪 的一种新的同位素 的一种新的同位素 |
下列各组的电极材料和电解液,不能组成原电池的是
| A.铜片、石墨棒,蔗糖溶液 | B.锌片、石墨棒,硫酸铜溶液 |
| C.锌片、铜片,稀盐酸 | D.铜片、银片,硝酸银溶液 |
下列化学用语书写正确的是
A.氮气的电子式: |
B.硫原子的结构示意图: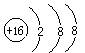 |
C.溴化钠的电子式: |
D.水分子的结构式:H—O—H |