将51.2g铜恰好完全溶于一定量的硝酸溶液中,得到硝酸铜溶液,收集到氮的氧化物(含NO、NO2、N2O4)的混合物共17.92L(标准状况),在这些气体中通入VL(标准状况)的氧气后用一定量的氢氧化钠溶液吸收,结果剩余2.24L(标准状况)气体。则通入氧气的体积V为
| A.7.28L | B.8.96L | C.11.20L | D.16.8L |
关于SiO2晶体的叙述中,正确的是( )
| A.通常状况下,60 g SiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数) |
| B.60 g SiO2晶体中,含有2NA个Si—O键 |
| C.晶体中与同一硅原子相连的4个氧原子处于同一四面体的4个顶点 |
| D.SiO2晶体中含有1个硅原子,2个氧原子 |
根据热化学方程式:S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ·mol-1,分析下列说法正确的是()
| A.S(s)+O2(g)===SO2(g),反应放出的热量大于293.23 kJ·mol-1 |
| B.S(g)+O2(g)===SO2(g),反应放出的热量小于293.23 kJ·mol-1 |
| C.1 mol SO2的化学键断裂吸收的能量总和大于1 mol 硫和1 mol氧气的化学键断裂吸收的能量之和 |
| D.1 mol SO2的化学键断裂吸收的能量总和小于1 mol硫和1 mol氧气的化学键断裂吸收的能量之和 |
PASS是新一代高效絮凝净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是()
| A.它们的原子半径依次增大 | B.WY2能与碱反应,但不能与任何酸反应 |
| C.Z与Y形成的化合物是一种耐高温材料 | D.热稳定性:X2R >X2Y |
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
| A.AgNO3 | B.Na2SO4 | C.CuCl2 | D.KCl】 |
为体现“城市让生活更美好”的主题,上海市政府承诺世博园区内交通“零排放”、园区周边交通“低排放”。2010年4月15日新能源车交车仪式在世博园举行,该车装着“绿色心脏”——质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )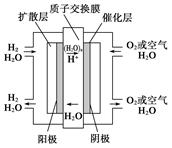
| A.通入氧气的电极发生氧化反应 |
| B.通入氢气的电极为正极 |
C.总反应式为O2+2H2 2H2O 2H2O |
| D.正极的电极反应式为O2+4H++4e-===2H2O |