下图是实验室制备1,2—二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略)。
有关数据列表如下:
| |
乙醇 |
1,2-二溴乙烷 |
乙醚 |
| 状态 |
无色液体 |
无色液体 |
无色液体 |
| 密度/g/cm3 |
0.79 |
2.2 |
0.71 |
| 沸点/℃ |
78.5 |
132 |
34.6 |
| 熔点/℃ |
一l30 |
9 |
-1l6 |
请按要求回答下列问题:
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:____________________________________________________________。
(2)气体发生装置使用连通滴液漏斗的原因_________________________________________。
(3)装置D中品红溶液的作用是_______________;同时B装置是安全瓶,监测实验进行时E中是否发生堵塞,请写出堵塞时的现象_______________________________________。
(4)反应过程中应用冷水冷却装置E,其主要目的是___________________________;但又不能过度冷却(如用冰水),其原因是_____________________________________________。
(5)判断该制备反应已经结束的方法是__________________;结果学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是_______________________________________。
(6)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,判断改用四氯化碳液体是否可行______(填“是”或“否”),其原因是____________________________。
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。其实验步骤为:
附表 相关物质的沸点(101 kPa)
| 物质 |
沸点/℃ |
物质 |
沸点/℃ |
| 溴 |
58.8 |
1,2二氯乙烷 |
83.5 |
| 苯甲醛 |
179 |
间溴苯甲醛 |
229 |
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2二氯乙烷和苯甲醛充分混合后,升温至60 ℃,缓慢滴加经浓H2SO4干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置中冷凝管的主要作用是________,锥形瓶中的溶液应为________。
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为____________。
(3)步骤2中用10% NaHCO3溶液洗涤有机相,是为了除去溶于有机相的____________(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是___________________。
(5)步骤4中采用减压蒸馏(在蒸馏装置上连接真空泵,使系统内压降低,从而使液体化合物在较低温度下沸腾而被蒸出)技术,是为了防止____________。
某化学小组拟采用如图所示装置(夹持和加热仪器已略去)来电解4mol/l食盐水,并用电解产生的H2还原CuO粉末,以此来测定Cu的相对原子质量。同时用产生的氢气与一氧化碳合成二甲醚。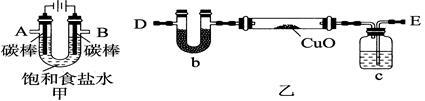
请回答下列问题:
(1)配制本实验用到的4mol/LNaCl溶液250ml需NaCl固体质量 克,定容时俯视容量瓶将使所配溶液浓度 4mol/L(“大于”、“等于”、“小于”)
(2)为完成上述实验,正确的连接顺序为A连______________(填字母);电解发生的总的离子反应方程式为___ _____ 。
(3)通入氢气一段时间后,对硬质玻璃管里的CuO粉末加热前,需要进行的操作___________________。
(4)精确称量硬质玻璃管的质量为a g,放入CuO后,精确称量硬质玻璃管和CuO的总质量为b g,实验完毕后:通过精确称量U形管反应前后的质量,来确定生成水的质量d g,进而确定Cu的相对原子质量。利用U型管质量判断不再有水生成的方法是 本实验有明显不足之处,请指出并提出改进意见 。若不改进将使测定结果 (“偏高”、“偏低”、“无影响”)。根据以上数据计算铜的相对原子质量______________。
己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:
| 物质 |
密度(g/cm3) |
熔点 |
沸点 |
溶解性 |
| 环己醇 |
0.962g/cm3 |
25.9℃ |
160.8℃ |
20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 |
1.360g/cm3 |
152℃ |
337.5℃ |
在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |

实验步骤如下:
I.在三口烧瓶中加入16 mL 50%的硝酸(密度为l.3lg/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃一90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ,趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)本实验所用50%的硝酸物质的量浓度为__________。滴液漏斗的细支管a的作用是 。
(2)仪器b的名称为____ 使用时要从________(填“上口”或“下口”)通入冷水。
(3)NaOH溶液的作用是__________,溶液上方倒扣的漏斗作用是 。
(4)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(5)进行该实验时要控制好环己醇的滴入速率,防止反应过于剧烈,否则可能造成较严重的后果,试列举两条可能的后果: 。
(6)为了除去可能的杂质和减少产品损失,可分别用__________和____________洗涤晶体。
在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O] (式量为392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(1)为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是 .
A.用冷水洗
B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗
D.用90%的乙醇溶液洗
(2)为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 |
第一次 |
第二次 |
第三次 |
| 消耗高锰酸钾溶液体积/mL |
25.52 |
25.02 |
24.98 |
滴定过程中发生反应的离子方程式为 。
滴定终点的现象是 。
通过实验数据计算的该产品纯度为 (用字母ac表)。上表中第一次实验中记录数据明显大于后两次,其原因可能是 (填符号)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积,并检验氯气(氯气有毒,可以用NaOH溶液吸收,氯气可以和碘化钾反应生成碘单质)。
(1)A极发生的电极反应式是___________________,
B极发生的电极反应式是_______________________。
(2)设计上述气体实验装置时,各接口的正确连接顺序为:A接______、 ______接______ ; B接______ 、 ______接______ 。
(3)证明产物中有Cl2的实验现象是_________。
(4)已知电解后测得产生的H2的体积为44.8 mL(已经折算成标准状况),电解后溶液的体积为50 mL,此时溶液中NaOH的物质的量浓度为________。