下表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是
| pH |
c(CrO42—) |
c(HCrO4—) |
c(Cr2O72—) |
c(H2CrO4) |
| 4 |
0.0003 |
0.1040 |
0.4480 |
0 |
| 6 |
0.0319 |
0.0999 |
0.4370 |
0 |
| 7 |
0.2745 |
0.0860 |
0.3195 |
0 |
| 9 |
0.9960 |
0.0031 |
0.0004 |
0 |
A.铬酸第一级电离方程式为H2CrO4 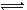 H++HCrO4—
H++HCrO4—
B.要得到CrO42—应控制溶液的pH>9
C.当电离达到平衡时,2v(正)(HCrO4—)= v(逆)(Cr2O72—)
D.该铬酸溶液的物质的量浓度约为1.00mol/L
溶液中存在有五种离子,其中各离子个数比Cl﹣:SO42﹣:Fe3+:K+:M=2:3:1:3:1,则M为
| A.CO32﹣ | B.Mg2+ | C.Na+ | D.Ba2+ |
据中央电视台报道,近年来我国的一些沿江城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列哪种分散系
| A.乳浊液 | B.溶液 | C.胶体 | D.悬浊液 |
氧化还原反应的本质是
| A.氧元素的得与失 | B.化合价的升降 |
| C.电子的转移 | D.分子中原子重新组合 |
下列各组中的离子,能在溶液中大量共存的是
| A.H+、Na+、CO32- | B.Cl-、Ba2+、SO42- |
| C.H+、OH-、SO42- | D.H+、Ag+、NO3- |
下列的离子方程式正确的是
| A.用大理石跟稀盐酸制二氧化碳:CO32—+2H+==H2O+CO2↑ |
| B.向氢氧化钡溶液中加硫酸溶液:SO42-+Ba2+= BaSO4↓ |
| C.硫酸溶液中加入Mg (OH)2:2H++ Mg(OH)2==Mg2+ +2H2O |
| D.铁与稀盐酸反应:Fe +6H+ ==2Fe3+ +3H2↑ |