实验:①0.1 mol/LAgNO3溶液和0.1 mol/LNaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol/L KI溶液,出现浑浊;③向沉淀c中滴加0.1 mol/LKI溶液,沉淀变为黄色。下列分析不正确的是
A. 浊液a中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl(aq)
Ag+(aq)+Cl(aq)
B. 滤液b中不含有Ag+
C. ③中颜色变化说明AgCl转化为AgI
D. 实验可以证明AgI比AgCl更难溶
ATP是细胞内直接的能源物质,可通过多种细胞途径产生(如下图所示)。以下说法正确的是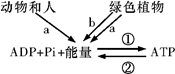
| A.a过程和b过程都有[H]的生成 |
| B.a过程和b过程都要在细胞器中进行 |
| C.O2由红细胞进入肝脏细胞的线粒体使肝脏细胞内的ADP含量迅速下降 |
| D.①②在物质和能量上都可成为互逆反应 |
阳光穿过森林空隙形成的“光斑”会随太阳移动和枝叶的摆动而移动。右图表示一株生长旺盛的植物在光斑照射前后光合作用过程中吸收CO2和释放O2有关的变化曲线,此曲线说明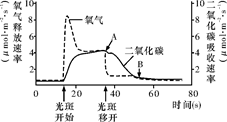
| A.光斑照射前光合作用无法进行 |
| B.光斑照射开始后,光反应和暗反应迅速同步增加 |
| C.光斑照射后O2释放曲线的变化说明暗反应对光反应有限制作用 |
| D.CO2曲线AB段变化说明进行暗反应与光照无关 |
科学家揭示出电压控制的钾通道,这些通道是负责K+进出细胞的看门蛋白质,它们在神经和肌肉细胞上的作用,与晶体管在计算机中的作用一样。这一成果从另一侧面证明了细胞膜具有
| A.免疫功能 | B.识别功能 |
| C.控制物质进出细胞的功能 | D.进行细胞间信息交流的功能 |
据报道,PBA和TUDCA两种化合物有助于糖尿病治疗,这两种药物可以缓解“内质网压力”(指过多的物质如脂肪积累到内质网中使其出错的状态)和抑制JNK基因活动,以恢复Ⅱ型糖尿病患者的正常血糖,并已对Ⅱ型糖尿病小鼠进行实验并获得成功。以下对此分析错误的是
| A.肥胖与Ⅱ型糖尿病的病因有关 |
| B.内质网功能出错影响了胰岛素的合成 |
| C.JNK基因活动受抑制是Ⅱ型糖尿病的另一病因 |
| D.Ⅱ型糖尿病小鼠胰岛素的合成和分泌与高尔基体有关 |
下列有关生物的共同特征的叙述,正确的是
| A.酵母菌、乳酸菌都是细菌,且都能进行有丝分裂,遗传都遵循遗传定律 |
| B.酵母菌、乳酸菌、硝化细菌都不含叶绿素,且都是分解者,都能进行有氧呼吸 |
| C.乳酸菌、硝化细菌、蓝藻都是原核生物,且都有细胞壁,体内含有DNA和RNA两类核酸分子 |
| D.乳酸菌、硝化细菌都是异养生物,在电镜下可观察到核糖体附着在内质网上 |