下列各组离子在指定溶液中,一定有大量共存的是
| A.pH=0的溶液中:Na+、[Al(OH)4]-、K+、NH4+ |
| B.由水电离出的c(H+)=10-12mol/L的溶液中:C1-、HCO3-、NH4+、SO32- |
| C.加入铝能离出H2的溶液中:Mg2+、NH4+、C1-、SO42- |
| D.滴加石蕊试液显蓝色的溶液:K+、Ba2+、NO3-、OH- |
将质量相等的Ag片和铂片插入硝酸银溶液(足量)中,银片与电源正极相连,铂片与电源负极相连。以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min。下列为表示银电极的质量、铂电极的质量、电解池中产生气体的质量和电解时间的关系图,正确的是
A. |
B.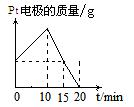 |
C. |
D. |
已知反应:C2H2(g)+H2(g) C2H4(g)在降低温度时平衡向右移动,则下列两个反应: C(s)+1/2H2(g)
C2H4(g)在降低温度时平衡向右移动,则下列两个反应: C(s)+1/2H2(g) 1/2C2H2(g);ΔH=-Q1
1/2C2H2(g);ΔH=-Q1
C(s)+H2(g) 1/2C2H4(g);ΔH=-Q2(Q1、Q2均为正值),
1/2C2H4(g);ΔH=-Q2(Q1、Q2均为正值),
“Q值”大小比较正确的是
| A.Q2>Q1 | B.Q1>Q2 | C.Q2=Q1 | D.不能确定 |
有关晶体的下列说法正确的是
| A.干冰属于分子晶体,其晶体中存在氢键 |
| B.在晶体中,只要有阴离子就一定有阳离子 |
| C.不含任何化学键的晶体是不存在的 |
| D.分子晶体的熔点一定低于金属晶体 |
工业上用二氧化锰制备高锰酸钾可分两步进行。
(1)二氧化锰与氢氧化钾共熔,并通入氧气: ;
;
(2)电解锰酸钾溶液: 。
。
下列说法正确的是
| A.上述物质中,氧化性:KMnO4> K2MnO4 >O2 |
| B.上述过程中,每生成1 mol KMnO4需转移6 mol 电子 |
| C.电解时,KMnO4在阳极区生成 |
| D.电解时,阴极周围pH减小 |
下列说法正确的是
| A.测定中和热时,所用稀NaOH溶液和HCl的物质的量恰好相等,以减小实验误差 |
| B.NaHSO4固体受热变为熔融状态(未发生化学反应),需要克服的作用力有:离子键和共价键 |
| C.在Fe(OH)3胶体中通电,一段时间后,阴极附近颜色加深 |
| D.用蒸馏的方法分离淀粉溶液与Cu(OH)2悬浊液的混合物 |