同学们对实验“煅烧石灰石”展开深入探究。
(1)煅烧石灰石。可观察到石灰石的表面 。
(2)为证明石灰石已分解,三位同学从其他角度设计方案如下: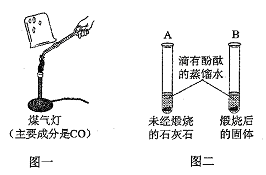
Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式__ __。
II.乙同学按图二所示进行试验,观察到B中液体变 色,A中实验的作用 。
III.丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO2的质量),证明石灰石已分解。
IV.大家认为甲同学的方案不合理,请分析原因 _ 。
(3)为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生mg气体,结合上述数据计算可知,丙所取的这块石灰石中含碳酸钙 _ mol(用m表示)。
竹子是“有节、中空、四季常绿”的植物.同学们对竹子中的气体成分展开了探究,测定其成分.
收集竹子中的气体.
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体.
小刚提出:可用注射器从竹子中抽取气体.
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验.
检验气体中是否含有二氧化碳气体.
测定氧气含量.
【查阅资料】红磷的着火点为240℃,白磷的着火点为40℃.
【设计实验】同学们设计了如下图所示的方案一和方案二来测定氧气含量.
【进行实验】按上述两个方案进行多次实验.
【反思与评价】
a.实验中磷的量应为足量,原因是 .
b.两个方案的实验测定结果不同,测定结果比较准确的是方案 ,原因是 .
c.经过A、B两组同学的实验,A组测得的含氧量总是大于B组的,你认为原因是 .
下列装置用于实验室中CO2的制备、净化、检验,最后收集一瓶干燥的CO2。请回答下列问题:
(1)对实验室制取二氧化碳药品选择的探究实验,记录如下:
| 组别 |
药品 |
实验现象 |
| ① |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
| ② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
| ③ |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
从制取和收集的角度分析,一般选择第 (填序号)组药品,所发生反应的化学方程式为 。
(2)C装置用于检验二氧化碳气体,则C中所盛放的物质是 ,发生反应的化学方程式是 。
(3)反应过程中将弹簧夹关闭,在A中观察到的现象是 。
(4)E收集方法说明二氧化碳具有的物理性质是 。
竹子是“有节、中空、四季常绿”的植物。同学们对竹子中的气体成分展开了探究,测定其成分。
(1)收集竹子中的气体。
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体。
小刚提出:可用注射器从竹子中抽取气体。
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验。
(2)检验气体中是否含有二氧化碳气体。
| 实验步骤 |
实验现象 |
实验结论及解释 |
| 向所取气体中加入 |
|
有二氧化碳。 |
(3)测定氧气含量。
【查阅资料】红磷的着火点为240 ℃,白磷的着火点为40 ℃。
【设计实验】同学们设计了如下图所示的方案一和方案二来测定氧气含量。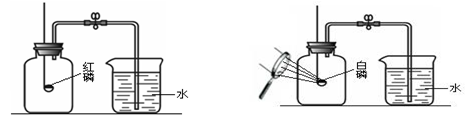
方案一方案二
【进行实验】按上述两个方案进行多次实验。
【反思与评价】
a.实验中磷的量必须______________,原因是 。
b.两个方案的实验测定结果不同,测定结果比较准确的是方案_______________,原因是 。
c.经过A、B两组同学的实验,A组测得的含氧量总是大于B组的,你认为原因是 。
实验设计是化学实验的重要环节。请根据下列实验要求回答相关问题:
【活动与探究一】收集不同体积比例的二氧化碳和一氧化碳混合气体。
方案一:如图所示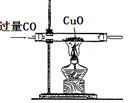
(1)请写出硬质玻璃管中发生反应的化学方程式 :
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是 。
方案二:根据如右图装置所示请回答下列问题:
(提示:饱和NaHCO3溶液的作用是除去HCl气体,部分夹持装置及导管已略去)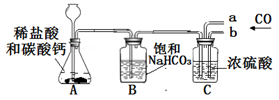
(1)写出装置A中发生反应的化学方程式: 。
(2)CO气体应由 (填“a”或“b”)通入,在C中混合后,由另一导管导出。
(3)装置C中浓硫酸的两点主要作用:
①干燥气体,减少实验误差;② 。
【活动与探究二】测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量。②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。③整理相关数据如下表,计算出钙片中碳酸钙的质量分数。
| 反应前总质量(克) |
275.58 |
| 反应后总质量(克) |
274.92 |
| 反应前后质量差(克) |
0.66 |
| 容器内气体质量差(克) |
m |

(1)该实验中,如果装置中不加固态干燥剂(吸水不吸二氧化碳),则最终所算得钙片中碳酸钙的质量将_____________________(填“偏大”“偏小”或“不变”)。
(2)反应前容器内是空气(密度为ρ1),反应后全部是CO2(密度为ρ2)。则反应前后
容器(容积为V)内的气体质量差m为 。(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。(钙片中的其它成分不与盐酸反应)
汽油主要组成元素是碳和氢,发动机中汽油与空气参与了一系列反应.学习小组为了探究某汽车所排放气体的成分,进行如下实验.
【猜想】
该气体可能含有 、 及少量的CO、NO和NO2等.你猜想含有这些气体的依据是 。
【查阅资料】
①NO是无色无味、难溶于水的有毒气体,NO2是红棕色、有刺激性气味的有毒气体。
②一氧化氮遇到氧气发生反应:2NO+O2═2NO2;
二氧化氮通入水中发生反应:3NO2+H2O═2HNO3+NO.
③CO和NO均可使新鲜血液变质而使颜色变暗.
【实验探究】
| 实验步骤 |
实验现象 |
实验结论及化学方程式 |
| (1)用球胆收集汽车排出气体 |
-------- |
-------- |
| (2)闻该气体气味 |
有刺激性气味 |
该气体中可能含有 |
| (3)将该气体通入足量澄清石灰水中 |
有白色沉淀生成 |
该气体中一定含有 ,生成白色沉淀的化学方程式是 。 |
(4) |
C中新鲜血液颜色变暗;D中有红棕色气体产生。 |
该气体中,除了(3)所确定的成分外,下列有关其余成分的说法一定不正确的是 ①只含NO ②只含NO2 ③只含CO ④含NO和NO2 ⑤含CO和NO2 ⑥含CO和NO ⑦含CO、NO和NO2 |
| (5)将(4)中C导出的气体通入 |
观察到 . |
该气体中一定含有CO |
【计算】将汽车排放的废气经过处理只含二氧化碳和一氧化碳,若用10g这种气体通过足量的氧化铁,高温一段时间后收集到12.4g气体,则10g气体中二氧化碳的质量为 。