下列化学方程式的书写及说明都正确的是
A.一氯丙烷与NaOH乙醇溶液共热:CH3CH2CH2Cl + NaOH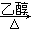 CH3CH2CH2OH + NaCl卤代烃水解得醇 CH3CH2CH2OH + NaCl卤代烃水解得醇 |
B.乙醇与浓硫酸共热到140℃:C2H5OH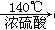 CH2=CH2↑+ H2O实验室制乙烯 CH2=CH2↑+ H2O实验室制乙烯 |
C.将灼热的铜丝伸入盛有无水乙醇的试管中:2CH3CH2OH + O2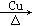 2CH3CHO乙醇可以被催化氧化得乙醛 2CH3CHO乙醇可以被催化氧化得乙醛 |
D.向苯酚钠中通入少量CO2: + CO2 + H2O → + CO2 + H2O → 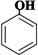 + NaHCO3碳酸的酸性比苯酚强 + NaHCO3碳酸的酸性比苯酚强 |
下列说法正确的是
| A.在一定温度下的AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数 |
| B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,[Ag+]=[Cl-],且Ag+和Cl-浓度的乘积等于1.8×10-10mol2·L-2 |
| C.温度一定时,在AgCl饱和溶液中,Ag+和Cl-浓度的乘积是一个常数 |
| D.向饱和AgCl溶液中加入盐酸,Ksp变大 |
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是
| A.将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,盐酸所加的水量多 |
| B.盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C.0.1mol·L-1醋酸钠溶液的pH>7 |
| D.相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
下列说法正确的是
| A.食盐溶液中除去SO42- 最合适的试剂是Ba(NO3)2 |
| B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C.25 ℃时,用醋酸溶液中和等浓度NaOH溶液至pH=7,VCH3COOH<VNaOH |
| D.AgCl易转化为AgI沉淀且Ksp(AgX)=[Ag+]·[X-],故Ksp(AgI)<Ksp(AgCl) |
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是
| A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-===Al(OH)3↓ |
| B.加水稀释后,溶液中c(NH4+)·c(OH-)变大 |
| C.用HNO3溶液完全中和后,溶液不显中性 |
| D.其溶液的pH=13 |
锌与很稀的硝酸反应4Zn + 10HNO3 = 4Zn(NO3)2 + NH4NO3 + 3H2O。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为
| A.2.5 mol | B.1 mol | C.0.5 mol | D.0.25 mol |