煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g)  H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
试回答下列问题:
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| |
n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
| A |
1 |
5 |
2 |
3 |
| B |
2 |
2 |
1 |
1 |
| C |
3 |
3 |
0 |
0 |
| D |
0.5 |
2 |
1 |
1 |
| E |
3 |
1 |
2 |
1 |
(2)在1L密闭容器中通入10 molCO和10 mol水蒸气,在500℃下经过30s达到平衡,则30s内CO的平均反应速率为 。
(3)已知在一定温度下,C(s)+CO2(g) 2CO(g)平衡常数K;K的表达式 ;
2CO(g)平衡常数K;K的表达式 ;
C(s)+H2O(g) CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g)平衡常数K2;
H2(g)+CO2(g)平衡常数K2;
则K、K1、K2之间的关系是: ;
(4)某温度下C(s)+CO2(g) 2CO(g)能判断该反应达到化学平衡状态的依据是________。
2CO(g)能判断该反应达到化学平衡状态的依据是________。
A.c(CO2)=c(CO) B.K不变 C.容器中的压强不变
D.v正(CO)=2v正(CO2) E.c(CO)保持不变 F.混合气体相对分子质量不变
(5)如图1所示,在甲、乙两容器中都充入1molC和1molCO2,并使甲、乙两容器初始容积相等。在相同温度下发生反应C(s)+CO2(g) 2CO(g),并维持反应过程中温度不变。已知甲容器中
2CO(g),并维持反应过程中温度不变。已知甲容器中
CO2的转化率随时间变化的图像如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图像。
图1 图2
按如图所示装置进行电解,在通电一段时间后,铁电极的质量增加。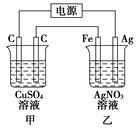
(1)乙杯中,两极发生的电极反应式是
________________________________________________________________________
________________________________________________________________________。
(2)甲杯中发生反应的化学方程式是
________________________________________________________________________
________________________________________________________________________。
(3)C—C—Fe—Ag四个电极上析出或溶解物质的物质的量比是________。
普通泡沫灭火器内的玻璃筒里盛Al2(SO4)3溶液,铁筒中盛NaHCO3溶液,其反应的离子方程式是
________________________________________________________________________
________________________________________________________________________。
不能把Al2(SO4)3溶液盛在铁筒中的原因是
________________________________________________________________________
________________________________________________________________________。
不用溶解度较大的Na2CO3代替NaHCO3的原因是
________________________________________________________________________。
水解反应是广泛存在的一类反应,盐的水解即为一例。越弱越水解是盐水解的重要规律,如NaCl不水解,MgCl2水解,而同浓度的AlCl3水解程度比MgCl2高。从同周期中元素金属性递变规律看H4SiO4的酸性更弱,因而SiCl4水解更完全。
(1)请写出下列化学方程式:
①SiCl4水解:
________________________________________________________________________;
②PCl5水解:
________________________________________________________________________。
(2)Mg3N2及CaC2与水反应也可看做水解,注意以下规律:
Mg3N2+6H2O===3Mg(OH)2↓+2NH3↑
CaC2+2H2O===Ca(OH)2+C2H2↑
写出下列化学方程式:
①Ca3P2与水反应:
________________________________________________________________________;
②Mg3C2与水反应:
________________________________________________________________________。
已知25 ℃时0.1 mol·L-1醋酸溶液的pH约为3,向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)上述两种解释中________(填“甲”或“乙”)正确。
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的________(填写编号字母),然后测定溶液的pH。
| A.固体CH3COOK | B.固体CH3COONH4 |
| C.气体NH3 | D.固体NaHCO3 |
(3)若________(填“甲”或“乙”)的解释正确,溶液的pH应________(填“增大”、“减小”或“不变”)(已知25 ℃ 时,CH3COONH4溶液呈中性)。
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有________种粒子。
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是________和________。
③溶液中n(CH3COO-)+n(OH-)-n(H+)=________mol。
装置如图1所示,三个连通的烧瓶里盛有二氧化氮和四氧化二氮的混合气体。然后用夹子夹住橡皮管,把左边的烧瓶放在热水里,把右边的烧瓶放在冰水(冷水)里,把中间的烧瓶放在室温水里,观察混合气体颜色的变化是:左边混合气体受热颜色变________,右边混合气体遇冷颜色变________,中间混合气体颜色无变化。
实验装置如图2所示,先将三个烧瓶分别放入盛有室温水的烧杯里,可以观察到混合气体颜色无变化,接着向左边烧杯里加入固体氢氧化钠,向右边烧杯里加入固体NH4NO3,不断搅拌直至溶液饱和,可以看到,随着固体的加入左边的混合气体颜色变________,右边的混合气体颜色变________,中间混合气体颜色不变。