材料是人类赖以生存的重要物质基础。铜、镍等金属材料在现代社会中有着重要应用。请回答下列问题:
(1)铜在元素周期表中的位置为 ,镍的基态电子排布式为 。
(2)在配离子[Ni(NH3)4]2+中,配体中N元素与它相邻的C和O元素的第一电离能由大到小的顺序为 ,这三种元素电负性由大到小的顺序为 ;配体NH3中N原子的杂化方式为 。
(3)据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积,如图,晶体中每个镁原子周围距离最近的镍原子有 个,若已知晶胞的边长为a pm,阿伏伽德罗常数为NA,则该晶体的密度的数学表达式为 g•cm-3(用a和NA表示,只列式,可不用化简)。
(12分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是_______
(2)X与W组成的化合物中存在_______键(填“离子”“共价”)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为____________________________________________________ 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A。
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式_________________________________________
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式:
____________________________________________________ 。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
A.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
B.B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为______________ 。
② 已知1 mol·L—1 100mL B的溶液能与1 mol·L—1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式____________________________________________________。
(8分)已知A、B、C、D是中学化学中常见的四种不同粒子 .它们之间存在如下图所示的转化关系:
.它们之间存在如下图所示的转化关系: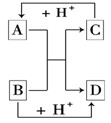
(1)如果A、B、C、D均是10电子的粒子,请写出:
A的结构式_______; D的电子式_______;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,
请写出:
①A与B在溶液中反应的离子方程式 :
:
________________________________________________________
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
(8分) (1)1971年美国的斯图杰尔和阿佩里曼在0℃ 以下将氟气从细冰末上通过,成功地合成了一直认为不存在的氟的含氧酸——次氟酸。
①写出次氟酸的结构并标出各元素的化合价__________________;
②次氟酸刹那间被热水分解得到既可表现氧化性(对NaI)又可表现还原性(对KMnO4)的溶液,写出次氟酸分解 反应的化学方程式:____________________________。
反应的化学方程式:____________________________。
(2) 氰(CN)2的化学性质与卤素(X2)很相似称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。氰的氧化性比溴弱、比碘强。
①HCN分子中含有4个共价键,写出HCN的结构式:_______ ;
②下列有关方程式不正确的是____________。
A. (CN)2+2NaOH===NaCN+NaCNO+H2O (CN)2+2NaOH===NaCN+NaCNO+H2O |
|
| B.MnO2+4HCN===Mn(CN)2+(CN)2+2H2O | C.I2+2KCN===2KI+(CN)2 |
| D.向NaBr(aq)和KCN(aq)中加入少量Cl2:Cl2+2NaBr===2NaCl+Br2 |
(10分)类推法是科学学习的重要方法之一
(1)下列类推结论正确的是:
| 类比对象 |
结论 |
|
| A |
Cl2+H2O HCl+H HCl+H ClO ClO |
I2+H2O HI+HIO HI+HIO |
| B |
C+2CuO  2Cu+CO2↑ 2Cu+CO2↑ |
C+SiO2  Si+ CO2↑ Si+ CO2↑ |
| C |
Na2O+H2O ="=" 2NaOH |
CuO+H2O ="=" Cu(OH)2 |
| D |
Ca(ClO)2+CO2+H2O="=" CaCO3↓+2HClO |
Ca(ClO)2+SO2+H2O="=" CaSO3↓+2HClO |
(2)在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质.请结合元素周期律完成下列问题:
| 元素 |
8O |
16S |
34Se |
52Te |
| 单质熔点(℃) |
-218.4 |
113 |
450 |
|
| 单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
| 主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
| 原子半径 |
逐渐增大 |
|||
| 单质与H2 反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
①硒的熔点范围可能是_______ ;②碲的化合价可能有_______ ;
③硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是 (填化学式);
④氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为___________________________________。
(8分)通过简单地推理或计算填空:
(1)X原子有两个电子层,它能与最活泼的金属Y形成Y3X的化合物,X是_______元素(写元素符号)。
(2)若某元素原子的电子层数和Na原子的相同,最外层电子数与F原子相同,则该元素的原子序数是_______。
(3)6C元素能够与某非金属元素R形成化合物CRn,已知CRx分子中各原子核外最外层电子总数为32,核外电子数总和为74。则R是_______元素(写元素符号),n=_______。
(4)有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
| 元素编号 |
元素特征信息 |
| A |
其单质是密度最小的物质 |
| B |
阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C |
其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D |
其氢氧化物和氧化物都有两性,与C同周期 |
| E |
与C同周期,原子半径在该周期最小 |
①写出E单质与A、B、C形成的化合物反应的化学方程式: ____________.
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:____________.