常温下,在c(H+)/c(OH−)=1×1012的溶液中,下列各组离子能大量共存的是
| A.Fe2+、Mg2+、NO3−、SO42− | B.Fe3+、Na+、Cl−、SCN− |
| C.NH4+、Al3+、NO3−、Cl− | D.Ca2+、K+、Cl−、HCO3− |
影响化学反应速率的因素很多,下列措施一定能提高反应速率的是()
| A.改变反应物用量 | B.减小压强 |
| C.降低温度 | D.升高温度 |
在以下4个反应中,铁元素的化合价变化与另外3个反应不同的是()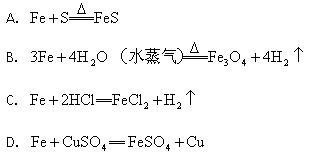
下列各组离子中,能在溶液中大量共存的是 .. ()
| A.H+Na+CO32- Cl- | B.Mg2+ Na+Cl- SO42- |
| C.K+ NH4+ SO42-OH- | D.Fe2+ Al3+ NO3-H+ |
下列物质中,能发生水解反应的是()
| A.苯 | B.乙酸 | C.蛋白质 | D.葡萄糖 |
下列化学用语表达正确的是()
A.S2-的结构示意图: |
B.NH3的结构式: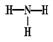 |
C.氯化钠的电子式: |
D.乙烯的结构简式:CH2CH2 |