工业上制备 BaC12 的工艺流程图如图所示:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得: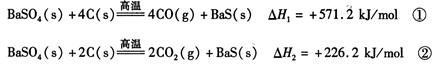
(1)反应C(s) + CO2(g) 2CO(g)的△H = kJ/mol
2CO(g)的△H = kJ/mol
(2)过滤过程中需要使用玻璃棒,玻璃棒的作用是 。
(3)盐酸溶解焙烧的固体后,产生的气体用过量 NaOH 溶液吸收,得到硫化钠溶液。 Na2S 水解的离子方程式为 。
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,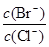 = 。[已知:
= 。[已知:
Ksp(AgBr) = 5.4×10─13 , Ksp(AgCl) = 2.0×10─10]
原高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或 Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:
(1)两支试管均产生大量气体,盛的试管中气体产生较快,盛的试管中气球变得更大;
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度有升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了下列热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3—(aq)+ H+(aq) ="===" H2O(l)+ CO2(g) △H>0
CO32—(aq)+ 2H+(aq) ="===" H2O(l)+ CO2(g) △H<0
甲下结论的方法是否正确(填“正确”或“不正确”)
(3)为研究是吸热还是放热反应,乙同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 |
试剂1 |
试剂2 |
混合 前温度 |
混合后最高 或最低温度 |
| ① |
35mL水 |
2.5g NaHCO3固体 |
20℃ |
18.5℃ |
| ② |
35mL水 |
3.2 Na2CO3固体 |
20℃ |
24.3℃ |
| ③ |
35mL稀盐酸 |
含2.5g NaHCO3的饱和溶液32.5mL |
20℃ |
19℃ |
| ④ |
35mL稀盐酸 |
含3.2g Na2CO3的饱和溶液23.1mL+10ml水 |
20℃ |
24.2℃ |
| ⑤ |
35mL稀盐酸 |
2.5gNaHCO3固体 |
20℃ |
16.2℃ |
| ⑥ |
35mL稀盐酸 |
3.2g Na2CO3固体 |
20℃ |
25.1℃ |
请你帮助填写相关内容:
通过上述实验可得出五条结论
a:NaHCO3的溶解是(吸热或放热)过程;
b:Na2CO3的溶解是(吸热或放热)过程;
c:NaHCO3的饱和溶液和盐酸的反应是(吸热或放热)反应;
d:Na2CO3的饱和溶液和盐酸的反应是(吸热或放热)反应;
e:NaHCO3固体与稀盐酸反应的反应热是由(填a→d的字母)的热效应之和。
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
(1)在这些元素中,化学性质最不活泼的是:(写元素符号)该原子结构示意图为。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是,碱性最强的化合物的化学式是:。
(3)最高价氧化物是两性氧化物的元素是;写出它的氧化物与氢氧化钠溶液反应的离子方程式。
(4)形成的单质硬度最大的元素是该单质的晶体类型为
(5)用电子式表示元素④与⑥形成的化合物:,该化合物属于化合物。(填 “共价”或“离子”)
(6)元素①与⑦形成的最简单的化合物的电子式是。该化合物属于化合物。(填 “共价”或“离子”)
(8分)用纯净的碳酸钙粉末跟稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如图所示,分析判断:________段化学反应速率最快。由该段图像说明:此反应属于________(填“吸热”或“放热”)反应
(2)为了减缓上述反应的化学反应速率欲向溶液中加入下列物质,你认为可行的是________(填字母代号)。
| A.蒸馏水 | B.NaCl固体 | C.NaCl溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率________________________________________________________________________
下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
族 周期 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
⑤ |
||||
| 3 |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
(1)请写出②的元素符号
(2)请写出③的最高价氧化物的电子式。
(3)比较⑤、⑥、⑧的原子半径由大到小的顺序为(用元素符号表示)
(4) 比较③、④、⑨的最高价含氧酸的酸性由强到弱的顺序是(用酸的化学式表示)。
比较③、④、⑨的最高价含氧酸的酸性由强到弱的顺序是(用酸的化学式表示)。
(5)写出在元素①-⑩中最高价氧化物对应水化物的最强碱与最强含氧酸之间的化学反应方程式
(6)⑦⑧两元素相比较,金属性较强的是(填名称),可以验证该结论的实验是(填编号)。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
常温下,甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
(1)甲硅烷含有的化学键是_________ ,其在固态时属于晶体。
(2)试比较甲硅烷与氨气的稳定性由大到小排列(化学式表示)
(3)现有①BaCl2、②金刚石、③NH4Cl、④Na2O2、⑤干冰、⑥甲硅烷(SiH4)六种物质,
含有共价键的化合物是(填序号)
(4)已知室温下1 g甲硅烷自燃生成SiO2和水并放出热量44.6 kJ,则其热化学方程式为。