金属镁及其化合物不仅在国防上有重要应用,在化学研究中也有广泛应用。
(1)某同学研究反应速率时用如下方法:取一段镁条,用砂纸擦去表面的氧化膜,使足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图所示。镁与盐酸反应的离子方程式为 ;在前4min内,镁条与盐酸的反应速率逐渐加快,在4 min之后,反应速率逐渐减慢,请简述其原因:_____________。
(2)向少量的Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,固体完全溶解,写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式 。
(3)Mg Al可形成原电池:
| 编号 |
电极材料 |
电解质溶液 |
电子流动 方向 |
| 1 |
Mg Al |
稀盐酸 |
Mg流向Al |
| 2 |
Mg Al |
NaOH溶液 |
|
根据上表中的实验现象完成下列问题:
①实验1中Mg为 极;
②实验2中电子流动方向 ,Al为 极,为什么? 。
某酯K是一种具有特殊香气的食用香料,广泛应用于食品和医疗中。其合成路线如下:
已知: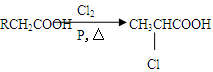
(1)E的含氧官能团名称是。
(2)试剂X是(填化学式);②的反应类型是。
(3)D的电离方程式是。
(4)F的分子式为C6H6O,其结构简式是。
(5)W的相对分子质量为58,1 mol W完全燃烧可产生3.0 mol CO2和3.0 mol H2O,且
W的分子中不含甲基,为链状结构。⑤的化学方程式是。
(6)G有多种属于酯的同分异构体,请写出同时满足下列条件的所有同分异构体的结构简式:。
① 能发生银镜反应且能与饱和溴水反应生成白色沉淀
② 苯环上只有两个取代基且苯环上的一硝基取代物只有两种
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列问题:
(1)已知:N2(g)+O2(g) = 2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)  2NH3(g)△H=-92.4kJ/mol
2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g) = 2H2O(g)△H=-483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为
。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) 2NH3(g)反应的影响。
2NH3(g)反应的影响。
实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图像中T2和T1的关系是:T2 T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2 的转化率最高的是(填字母)。。
③若容器容积为1L,在起始体系中加入1mol N2 ,n=3mol反应达到平衡时H2的转化率为60%,则此 条件下(T2),反应的平衡常数K=。保持容器体积不变,再向容器中加入1mol N2,3mol H2反应达到平衡时,氢气的转化率将
(填“增大”、“减”或“不变”)。
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
①一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g) 4NO2(g)+O2(g) ΔH>0下表为反应在T1温度下的部分实验数据
4NO2(g)+O2(g) ΔH>0下表为反应在T1温度下的部分实验数据
| t/s |
0 |
50 |
100 |
| c(N2O5)/mol·L—1 |
5.0 |
3.5 |
2.4 |
则50s内NO2的平均生成速率为。
②现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2。
写出石墨I电极上发生反应的电极反应式。
在电解池中生成N2O5的电极反应式为。
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,
B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
试回答:
(1)E元素在周期表中的位置为,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式。
(2) 由A、B、W三种元素组成的18电子微粒的结构简式为。
(3)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式。常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式。
(5) 元素D的单质在一定条件下,能与A单质化合生成一种氢化物DA,熔点为800℃。DA能与水反应放氢气,若将1mol DA和1 mol E单质混合加入足量的水,充分反应后生成气体的体积是L(标准状况下)。
肉桂醛在食品、医药化工等方面都有应用。
(1)质谱分析肉桂醛分子的相对分子质量为132。其分子中碳元素的质量分数为82%,其余为氢和氧。分子中的碳原子数等于氢、氧原子数之和。肉桂醛的分子式是。
(2) 肉桂醛具有下列性质:
请回答:
① 肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是。(本题均不考虑顺反异构与手性异构)
②Z不能发生的反应类型是。
| A.取代反应 | B.消去反应 | C.加成反应 | D.加聚反应 |
③Y与乙醇在一定条件下作用得到肉桂酸乙酯,该反应的化学方程式是。
④Y的同分异构体中,属于酯类且苯环上只有一个取代基的同分异构体有种,其中任意一种的结构简式是。
(3)已知
Ⅰ、醛与醛能发生反应,原理如下:
Ⅱ、合成肉桂醛的工业流程如下图所示(甲为烃):
请回答:
①甲的结构简式是。
②写出丙和丁生成肉桂醛的化学方程式是。
向2 L密闭容器中通入6mol气体A和6mol气体B,在一定条件下发生反应:
xA(g)+yB(g)=pC(g)+qD(g) 已知:平均反应速率v(C)=1/2v(A);反应2 min时,A的浓度减少了1mol/L,B的物质的量减少了3mol,有6mol D生成。回答下列问题:
(1)反应2 min内,v(A)=,v(B)=;
(2)该反应化学方程式中x:y:p:q=;
(3)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:反应速率(填“增大”、“减小”或“不变”),理由是。