在一定温度下,向饱和烧碱溶液中加入一定量的过氧化钠,充分反应后恢复到原温度,下列说法错误的是
| A.溶液中Na+数目减少,有固体析出 |
| B.溶液中Na+数目减少,有气体逸出, |
| C.溶液中H2O数目减少,溶质的质量分数增大 |
| D.溶液中H2O数目减少,溶质的质量分数未变 |
如图中,两电极上发生的电极反应如下: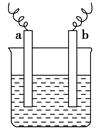
a极:Cu2++2e-=Cu;b极:Fe-2e-=Fe2+,则以下说法中不正确的是( )。
| A.该装置一定是原电池 |
| B.a极上一定发生还原反应 |
| C.a、b可以是同种电极材料 |
| D.该过程中能量的转换可以是电能转化为化学能 |
下列与金属腐蚀有关的说法,正确的是( )。
| A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图2中,往烧杯中滴加几滴KSCN溶液,溶液变血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 |
| D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。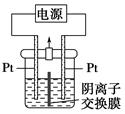
已知:3I2+6OH-=IO3—+5I-+3H2O
下列说法不正确的是 ( )。
| A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- |
| B.电解结束时,右侧溶液中含IO3— |
C.电解槽内发生反应的总化学方程式:KI+3H2O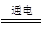 KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
如图所示,Ⓐ为直流电源,Ⓑ为浸透饱和氯化钠溶液和酚酞试液的滤纸,Ⓒ为电镀槽。接通电路(未闭合K)后发现Ⓑ上的c点显红色。为实现铁片上镀铜,接通K后,使c、d两点短路。下列叙述不正确的是 ( )。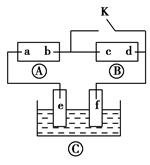
| A.b为直流电源的负极 |
| B.f极为阴极,发生还原反应 |
| C.e极材料为铁片,f极材料为铜片 |
| D.可选用CuSO4溶液或CuCl2溶液作电镀液 |
工业上可用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn,其工艺流程如下: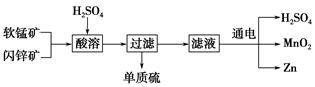
下列说法正确的是 ( )。
| A.酸溶时,MnO2作还原剂 |
| B.可用盐酸代替硫酸进行酸溶 |
| C.原料硫酸可以循环使用 |
| D.在电解池的阴极处产生MnO2 |