高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为,3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH下列叙述不正确的是
3Zn(OH)2 + 2Fe(OH)3 + 4KOH下列叙述不正确的是
| A.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化 |
| B.放电时负极反应为:Zn—2e— +2OH—= Zn(OH)2 |
C.充电时阳极反应为:Fe(OH)3 —3e— + 5 OH— = FeO + 4H2O + 4H2O |
| D.放电时正极附近溶液的碱性增强 |
把a、b、c、d四种金属片浸泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若a、b相连时,a为负极;c、d相连时,d为正极;a、c相连时,c上有气泡放出;b、d相连时,电子沿导线由d极流向b极。则这四种金属活动性顺序由大到小为
| A.a > b > c > d | B.a > c > d > b |
| C.c > a > b > d | D.b > d > c > a |
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ。有机物乙烷在一定条件下分解的反应可表示为: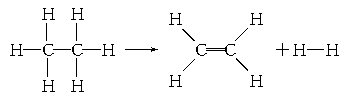
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是
| A.该反应放出251.2 kJ的热量 | B.该反应吸收251.2 kJ的热量 |
| C.该反应放出125.6 kJ的热量 | D.该反应吸收125.6 kJ的热量 |
下列关于吸热反应的说法正确的是
| A.凡需加热的反应一定是吸热反应 |
| B.只有分解反应才是吸热反应 |
| C.放热反应不用加热或点燃,常温下即可发生。 |
| D.CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 |
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。下列有关我们常用的元素周期表的说法正确的是( )
| A.元素周期表有七个横行,也是七个周期 |
| B.元素周期表有18个纵行,即有18个族 |
| C.短周期是指第一、二、三、四周期 |
| D.ⅠA族的元素全部是金属元素 |
将铜片与锌片用导线连接入插入稀硫酸中,锌片是()
| A.阴极 | B.阳极 | C.正极 | D.负极 |