对 Fe、Cl2、Al2O3、SiO2、NaClO、NaAlO2的分类正确的是
| A.能与碱反应的物质是Cl2、Al2O3、SiO2 |
| B.能与盐酸反应的物质是Fe、Al2O3、SiO2 |
| C.能与水反应的物质是Fe、Cl2、Al2O3 |
| D.具有两性的物质是Al2O3、SiO2、NaAlO2 |
.欲检验一瓶中装的是稀氨水,现用一沾有浓盐酸的玻棒靠近瓶口,为了使现象明显,可事先往瓶中加入下列哪种物质
①浓H2SO4 ②固体烧碱 ③固体P2O5 ④生石灰 ⑤固体NH4Cl ⑥固体食盐
| A.①② | B.②③④ | C.②④⑤ | D.①③⑥ |
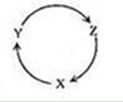
下列各组物质中,满足下图物质一步转化关系的选项是
| X |
Y |
Z |
|
| A |
Na |
NaOH |
NaHCO3 |
| B |
Cu |
CuSO4 |
Cu(OH)2 |
| C |
C |
CO |
CO2 |
| D |
Si |
SiO2 |
H2SiO3 |
下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 |
说明该钾盐是K2CO3 |
| B |
向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2 粉末,搅拌一段时间后过滤 |
除去MgCl2溶液中少量FeCl3 |
| C |
常温下,向饱和Na2CO3溶液中通入CO2气体,溶液中有固体析出 |
说明CO2可降低Na2CO3的溶解度 |
| D |
水蒸气通过足量Na2O2,产生的气体能使带火星的木条复燃 |
说明H2O具有还原性 |
下列叙述正确的是
| A.SO2具有还原性,故可作漂白剂 |
| B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| D.Fe在Cl2中燃烧生成FeCl3,故在与其它非金属反应的产物中的Fe也显+3价 |
除去下列括号内杂质的试剂或方法错误的是
| A.HNO3溶液(H2SO4),适量BaCl2溶液,过滤 |
| B.CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 |
| C.KNO3晶体(NaCl),蒸馏水,结晶 |
| D.Cl2(HCl),饱和食盐水,洗气 |