某同学利用下列装置进行浓硫酸和铜反应并验证二氧化硫的性质。按如图实验装置连接仪器和放置药品。加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出。实验结束后会看到两个试管的液体底部均有少量的白色固体。下列对该实验的现象分析或推断正确的是
| A.湿润的蓝色石蕊试纸先变红后褪色 |
| B.左边试管出现的白色固体是由于浓硫酸的脱水性所致 |
| C.从该实验的描述中可以体会出铜与浓硫酸的反应是一个放热反应 |
| D.本实验体现了二氧化硫的酸性、漂白性和弱氧化性 |
下列关于酸性氧化物、碱性氧化物、单质、混合物的分类中,正确的是
| 酸性氧化物 |
碱性氧化物 |
单质 |
混合物 |
|
| A |
干冰 |
Na2O |
金刚石 |
浓盐酸 |
| B |
CO |
Fe3O4 |
溴 |
漂白粉 |
| C |
SO2 |
Na2O2 |
石墨 |
福尔马林 |
| D |
SO3 |
Fe2O3 |
硫黄 |
FeSO4·7H2O |
【改编】关于Fe(OH)3胶体和MgCl2溶液说法正确的是
| A.都比较稳定,且无色透明 |
| B.可以用是否有丁达尔现象进行鉴别 |
| C.加入NaOH溶液都可产生白色沉淀 |
| D.胶体微粒不可透过滤纸,MgCl2溶液可以 |
某有机物的结构简式为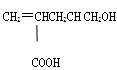 ,下列叙述不正确的是
,下列叙述不正确的是
| A.1mol该有机物能与足量金属钠反应放出1molH2 |
| B.能与乙醇发生酯化反应 |
| C.1mol该有机物在催化剂作用下最多能与1molH2发生还原反应 |
| D.1mol该有机物能与足量NaHCO3溶液反应放出2 molCO2 |
【原创】下列有关物质的应用说法正确的是
| A.可以用铝制槽罐车运输浓硫酸 |
| B.亚硝酸盐可以防腐,所以在食品中可以广泛使用 |
| C.洁厕灵和漂白粉都具有去污作用,一同使用效果会更 |
| D.治疗胃酸过多可以使用碳酸钠 |
【原创】常温常压下,向2L密闭容器中加入一定量的A和B气体,发生反应2A(g) + 2B(g) 2Q(g) + W(g)∆H=M kJ·moL−1,3min后,反应达到平衡,相关数据如下表:
2Q(g) + W(g)∆H=M kJ·moL−1,3min后,反应达到平衡,相关数据如下表:
| 反应时间/min |
n(A)/mol |
n(B)/mol |
| 0 |
4 |
4 |
| 0.5 |
3.2 |
|
| 2 |
2.4 |
|
| 3 |
1.0 |
下列说法正确的是
A.反应在前0.5min时,n(W)=0.6mol
B.2min时,反应的平均反应速率为V(Q)=0.48mol/L·s
C.相同温度条件下,向平衡后的容器中再充入2molQ和2molW时,v (正)> v (逆)
D.相同温度下,平衡时的平衡常数为18L·mol-1