大气固氮和合成氮是周氮的重要形式。下表是大气固氮和合成氨的部分K值:
| |
N2+O2 2NO 2NO |
N2+3H2 2NH3 2NH3 |
||
| 温度 |
25℃ |
2000℃ |
25℃ |
400℃ |
| 平衡常数K |
3.84×10-31 |
0.1 |
5×108 |
200 |
(1)大气固氮是_______(“吸热”、“放热”)反应;人工固氮对农业意义十分重大,根据表中数据,可推知合成氨最重要的研究方向是______________________________________。
(2)工业合成氨原料气的制备主要方法如下:
①以空气为原料制备N2,其方法是______________________________________。
②以焦炭和水为原料制备H2,反应原理为____________________、__________________。
H2中混有的CO可用醋酸亚铜氨溶液吸收,以防止合成氨时催化剂中毒:
CO(g)+Cu(NH3)2Ac(aq)  Cu(NH3)2AC·CO(aq)+Q(Q>0)
Cu(NH3)2AC·CO(aq)+Q(Q>0)
要从除杂后的溶液中“再生”出醋酸亚铜氨,可________(“升”“降”)温、____(“增”“降”)压。
(3)液氨和水类似,也能自离解(电离):NH3+NH3 NH4++NH2-。
NH4++NH2-。
①液氨的离子积可以表示为________________。
②25℃时,液氨的离子积K=1.0×10-30。若将NaNH2固体加入液氨中,则所得溶液中不存在的关系式是(设温度保持不变)_________ (选填编号)
a.c(Na+)=c(NH2-) b.c(NH4+)·c(NH2-)=1.0×10-30 c.c(NH2-)> c(NH4+)
(4)若在液氨中NaNH2和NH4Cl都能完全电离,则用标准NaNH2液氨溶液滴定未知浓度NH4Cl液氨溶液时,反应的离子方程式为_______________________。
科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是。(选填字母)
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |
(2)用水分解获得氢气的能量变化如右图所示,表示使用催化剂是曲线。该反应为(放热还是吸热)反应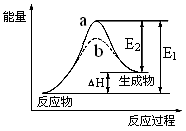
(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式:。
(4)利用氢气和CO合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g)的ΔH=
CH3OCH3(g) + CO2 (g)的ΔH=
(5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验: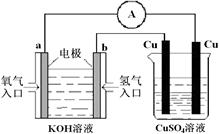
①氢氧燃料电池中,正极的电极反应式为。
②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为
L。
(6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式。
氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。
(1)检验氧化铜被氢气充分还原后,所得产物中是否含有氧化亚铜的的方法是:
;
(2)现有8 g氧化铜被氢气充分还原后,得到红色固体6.8克,其中含单质铜与氧化亚铜的物质的量之比是;
(3)若将6.8 g上述混合物全部溶解在稀硝酸中,
①写出Cu2O与稀硝酸反应的离子方程式;
②如果所得溶液体积为200mL,所得溶液的物质的量浓度为mol/L;
(4)将上述所得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体23.68 g。经分析,原溶液中的Cu2+有20%残留在母液中。求所得晶体的化学式(要求:写出本小题的计算过程)。
化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成: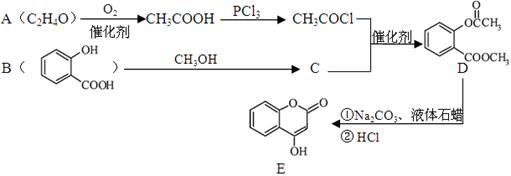

(1)A中含有的官能团名称为。
(2)C转化为D的反应类型是。
(3)写出D与足量NaOH溶液完全反应的化学方程式。
(4)1摩尔E最多可与摩尔H2加成。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式。
A.能发生银镜反应。 B.核磁共振氢谱只有4个峰。
C.能与FeCl3溶液发生显色反应,水解时每摩尔可消耗3摩尔NaOH。
(6)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化。
苯甲酸苯酚酯(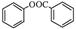 )是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
)是一种重要的有机合成中间体。试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。
合成路线流程图示例如下: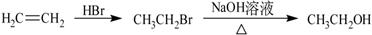
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下: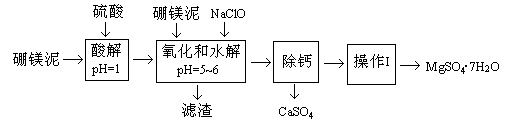
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式。在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法。
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) |
40 |
50 |
60 |
70 |
| MgSO4 |
30.9 |
33.4 |
35.6 |
36.9 |
| CaSO4 |
0.210 |
0.207 |
0.201 |
0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤、。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为。
工业上制取铝的流程如下:
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A,B,C,D,E。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| Al2O3 |
Fe2O3 |
Na2O |
|
| 铝土矿 |
55% |
16% |
0% |
| 赤泥 |
15% |
48% |
8% |
试求制取1t Al2O3所需铝土矿和苛性钠的质量。(写过程)