实验室制备乙酸丁酯,反应温度要控制在115℃~125℃之间,其他有关数据如下表:
| 物质 |
乙酸 |
1−丁醇 |
乙酸丁酯 |
98%浓硫酸 |
| 沸点 |
117.9℃ |
117.2℃ |
126.3℃ |
338.0℃ |
| 溶解性 |
溶于水和有机溶剂 |
溶于水和有机溶剂 |
微溶于水,溶于有机溶剂 |
与水混溶 |
关于实验室制备乙酸丁酯的叙述错误的是
A.不能边反应边蒸出乙酸丁酯的原因:乙酸丁酯的沸点高
B.不用水浴加热是因为:乙酸丁酯的沸点高于100℃
C.从反应后混合物分离出粗品的方法:用Na2CO3溶液洗涤后分液
D.由粗品制精品需要进行的一步操作:加吸水剂蒸馏
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是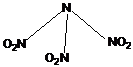
| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.15.2g该物质含有6.02×1022个原子 |
下列说法正确的是
| A.纤维素和淀粉遇碘水均显蓝色 |
| B.蛋白质、乙酸和葡萄糖均属电解质 |
| C.乙酸乙酯和食用植物油均可水解生成乙醇 |
| D.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 |
亚氨基羟(Li2NH)是一种储氢容量器,安全性好的固体储氢材料,其储氢原理可表示为
Li2NH+H2=LiNH2+LiH。
下列有关说法正确的是
| A.Li2NH中N的化合价是-1 | B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 | D.此法储氢和钢瓶储氢的原理相同 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、醛基、羧基 |
| C.含有羟基、羰基、羧基、酯基 |
| D.含有碳碳双键、苯环、酯基、羰基 |
下列各组有机物只用一种试剂无法鉴别的是
| A.乙醇、甲苯、硝基苯 | B.苯、苯酚、己烯 | C.苯、甲苯、环己烷 | D.甲酸、乙醛、乙酸 |