(本题共12分)
我国钾长石(KAlSi3O8)的资源比较丰富。工业上可用食盐和钾长石在一定条件下制备氯化钾:NaCl (l) +KAlSi3O8 (s)  KCl (l)+NaAlSi3O8 (s)。
KCl (l)+NaAlSi3O8 (s)。
完成下列填空:
(1)硅原子的最外层电子占据了 个轨道,有 种能量。
(2)氯化钠的熔点比氯化钾的 (填“高”或“低”),原因是 。
(3)把反应中涉及到的六种元素的原子半径按从小到大的顺序排列 。
(4)参与上述反应且位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,这种元素是 。
(5)为研究上述反应中钾元素的熔出率(液体中钾元素的质量占全部钾元素质量的百分率)与温度的关系,进行实验(氯化钠与钾长石投料的质量比为2:1),获得如下数据:
| 时间(h) 钾元素 温度 熔出率 |
1.5 |
2.5 |
3.0 |
3.5 |
4.0 |
| 830℃ |
0.481 |
0.575 |
0.626 |
0.669 |
0.685 |
| 890℃ |
0.579 |
0.691 |
0.694 |
0.699 |
0.699 |
| 950℃ |
0.669 |
0.714 |
0.714 |
0.714 |
0.714 |
①分析数据可以得出,该制备氯化钾的反应是 (填“放热”或“吸热”)反应。
②计算890℃时,氯化钠的平衡转化率 。(式量:KAlSi3O8–278 NaAlSi3O8 –262)
③950℃时,提高熔出钾的速率可以采取的措施是 (写出两种)。
对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ___________
(2)除去食盐溶液中的水 ___________
(3)淡化海水
(4)KCl中含有KClO3
I.小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式:。
II.氨气通入水中可制得氨水,氨水能使无色的酚酞变红。请写出实验室制取氨气的化学方程式:,
检验氨气的一种化学方法是:。
III.火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中氧化剂是;还原剂是。
用一定量的废铜制取胆矾有两种方法:第一种是取铜与浓H2SO4直接反应,化学反应方程式是;第二种是先将铜在空气中加热使之生成CuO,再与稀H2SO4反应。其中第种方法好,原因是。
(8分)用下面的原子或离子结构示意图的编号(A、B、C、D)填空: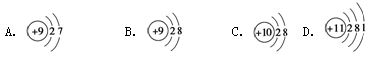
(1)核外电子层排布相同的是__________和___________;
(2)属于同种元素的是__________和__________;
(3)属于金属元素的是____________________;
(4)写出D参加化学反应后所得离子的结构示意图_______。
(16分,每空2分)
Ⅰ.某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。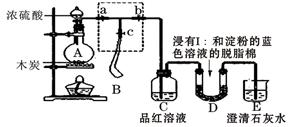
请回答下列问题
(1)对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。浓硫酸的危险警告标签是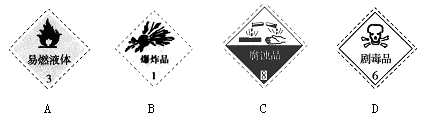
(2)装置A中发生反应的化学方程式为___________________________________。
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为_______________________________________;
(5)当D中产生_________________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
(6)若为检验浓硫酸与木炭在加热条件下生成的水蒸汽,可在装置___________________之间加上一个盛有无水CuSO4的硬质玻璃管。
Ⅱ.Cu与浓硫酸反应可得硫酸铜溶液。某学习小组将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气也可得硫酸铜溶液,其反应原理为2Cu+O2+2H2SO4="=" 2CuSO4+2H2O。现欲将12.8g铜完全溶解,加蒸馏水后得200 mL溶液。计算:
(7)参加反应的氧气在标准状况下的体积是___________________L。
(8)所得硫酸铜溶液的物质的量浓度是__________________mol/L。