某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化: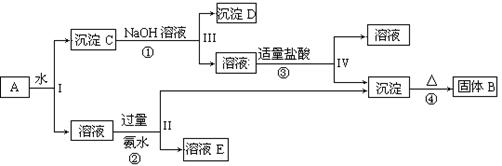
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出下列B、 D所含物质的化学式
固体B ;沉淀D 。
(3)写出①、②反应的离子方程式:
① ;② ;
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选。
A、B、C、D是短周期元素组成的非金属单质,其中B、C、D在常温常压下是气体。其转化关系如图(有关反应的条件及生成的H2O已略去),E是形成酸雨的污染物之一,F是常见的四原子10电子分子,化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。化合物J是由两种元素组成的18电子分子,分子中原子个数比为1:2,其相对分子质量为32,常温下为液体。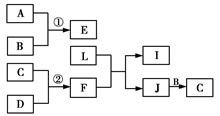
请按要求填空:
(1) A中所含元素在元素周期表中的位置为_________________。L中化学键的类型为
___________________(填“离子键”、“极性键”或“非极性键”)
(2)写出Cl2与NaOH溶液反应的化学方程式:__________________________。
(3)取16 g J在B中完全燃烧生成C,恢复至101 kPa、25℃,放出312 kJ热量。则J和B反应的热化学方程式为_______________________________________________________。
(4)写出将E通入L的碱性溶液中的离子方程式:________________。
(5)J-空气燃料电池是一种环境友好的碱性燃料电池,电解质溶液是20%~30% KOH溶液。该燃料电池的负极反应式为_________________________________________________。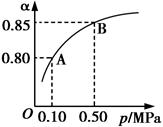
(6)对于反应2E+B 2G:
2G:
①某温度下,E的平衡转化率(α)与体系总压强(p)的关系如图所示。平衡状态由A变到B时,平衡常数K(A)________(填“>”“<”或“=”)K(B)。
②将一定量的E(g)和B(g)放入某固定体积的密闭容器中,在一定条件下,c(G)的变化如图所示。若在第5 min将容器的体积缩小一半后,在第8 min达到新的平衡(此时G的浓度为0.25mol/L)。请在图中画出此变化过程中G浓度的变化曲线。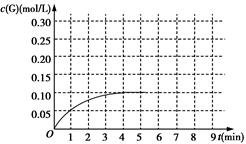
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。利用H2S废气制取氢气来的方法有多种
(1)高温热分解法
已知:H2S(g)  H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为0.2 mol·L-1测定H2S的转化率,结果见右图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=_____________;说明温度的升高,曲线b向曲线a逼近的原因:________________________________________________________
(2)电化学法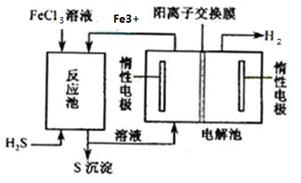
该法制氢过程的示意图如右。反应池中反应物的流向采用气、液逆流方式,其目的是___________;反应池中发生反应的化学方程式为_____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________________。
2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为: 2NO(g) + 2CO(g) 2CO2(g) +N2(g) 。在密闭容器中发生该反
2CO2(g) +N2(g) 。在密闭容器中发生该反
应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断: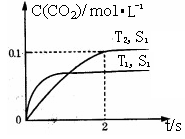
①该反应的△H0(填“>”、“<”)。
②在T2温度下,0~2s内的平均
反应速率v(N2)=" ______________" 。
③当固体催化剂的质量一定时,增大其表面积可提高
化学反应速率。若催化剂的表面积S1>S2,在上图中画出
c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到t1时刻达到平 衡状态的是____(填代号)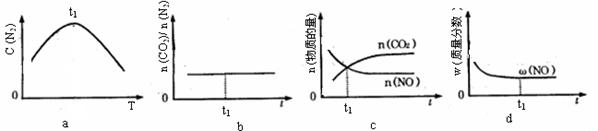
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。
例如: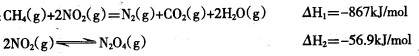
写出CH4 (g)催化还原N2O4(g)生成N2 (g)和H2O (g)的热化学方程式。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目 的。右图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式
为。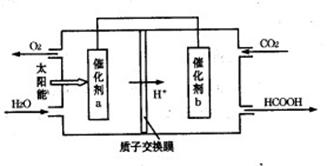
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的最高价氧化物对应的水化物的化学式为H2XO3 |
| Y |
Y是地壳中含量最高的元素 |
| Z |
Z元素的最外层电子数与电子层数相同 |
| W |
W的一种核素的质量数为28,中子数为14 |
(1) W位于元素周期表第周期第族;Z的离子结构示意图:_____________
四种元素的原子半径从大到小的顺序为:__________________________(用元素符号表示)
(2)氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称。
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是_____________
W的最高价含氧酸钠盐显_____性(填“酸”、“碱”或“中”),其用途是__________________
(4)常温下,不能与z单质发生反应的是_________(填序号)
a.CuSO4溶液 b.Fe2O3c.浓硫酸 d.NaOH e.Na2CO3固体
在25°、101kPa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,Z的燃烧热的热化学方程式是_________________________________。
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为、 、。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有、。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质的电子式为___________此化合物在酸性条件下与高锰酸钾反应的离子方程式为;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为。