已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )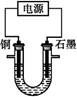
| A.铜电极连接电源正极 |
| B.黑色粉末X是铁粉 |
C.铜的相对原子质量的计算式是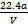 |
D.石墨电极上发生的反应是4OH--4e- O2↑+2H2O O2↑+2H2O |
设NA表示阿伏加德罗常数的数值,下列说法正确的是()
| A.2L 1mol·L-1 (NH4)2SO4溶液中含有4NA个铵根离子 |
B.100℃时,1L pH=6的纯水中,含1.0×10-6NA个 |
| C.电解CuCl2溶液,阴极析出6.4gCu时,转移的电子数为0.1NA |
| D.一定条件下用含1mol FeCl3的溶液制备Fe(OH)3胶体,产生NA个Fe(OH)3胶粒 |
下列物质溶于水时会破坏水的电离平衡,且属于电解质的是()
| A.氯气 | B.二氧化碳 | C.碘化钾 | D.醋酸钠 |
目前有研究表明,过氧乙酸对甲型H1N1流感病毒有较好的杀菌作用,这主要是利用了过氧乙酸的()
| A.酸性 | B.强氧化性 | C.还原性 | D.挥发性 |
相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO以及同温同体积同浓度的NaCN和NaClO,下列说法正确的是:
| A.影响水的电离平衡程度:NaCN>NaClO |
| B.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO > HCN |
| C.pH: HClO >HCN |
| D.电离程度:HCN>HClO |
下列各反应的离子方程式书写正确的是
| A.过氧化钠与水反应:O22−+ 2H2O = O2↑+ 4OH− |
| B.将氯气通入氯化亚铁溶液中:Fe2+ + Cl2 = 2Cl− + Fe3+ |
| C.氯气与水反应:Cl2+ H2O = 2H++ Cl−+ ClO− |
| D.氨水中滴加盐酸:H+ + NH3·H2O = NH4+ + H2O |