ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含ⅤA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)白磷单质中的P原子采用的轨道杂化方式是 。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为 。
(3)As原子序数为 ,其核外M层和N层电子的排布式为 。
(4)NH3的沸点比PH3 (填“高”或“低”),原因是 。
P 的立体构型为 。
的立体构型为 。
(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13。硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因 ;
②硝酸比亚硝酸酸性强的原因 。
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为 cm(用含有a的代数式表示)。在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如下页图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为 g(氧离子的半径为1.40×10-10 m)。 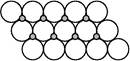
现在人们已能合成自然界并不存在的许多性能优良的有机高分子材料。由氯乙烯制取聚氯乙烯的反应属于_________反应。适合于合成聚氯乙烯的原料是_________
A CH4,Cl2 B CH3CH3,HCl C CH≡CH,HCl D CH2=CH2,HCl
近期国内外大量的研究表明,火灾中绝大多数人的第一死因并非高温烘烤或火烧,而是慌忙奔跑时吸入的烟雾中毒,且起火的建筑装修越豪华,这一特点越明显.聚氯乙烯是制作装修材料的最常用原料,失火后,随着火焰的剧烈跳动, 聚氯乙烯在不同的温度下,发生一系列的复杂化学变化,产生大量的有害气体,其大致过程如下:
请回答下列问题:
(1)火灾中由.聚氯乙烯产生的对人体有害气体,其化学成分主要有,你认为其中含量最大的为,在火灾现场,为防止气体中毒你应采取的防护措施是
(2)有机化学的基本反应类型有:
| A.加成反应 | B.消去反应 | C.取代反应 | D.重排反应4种,其中重排反应是指象CH2=CH-OH→CH3CHO的一类反应,请指出上述变化中下列所属的基本类型(填序号): |
①③
(3)在装修中广泛使用的粘合剂也是极易发生火灾的物质. 聚乙烯缩丁醛就是这样一种粘合剂,它是由聚乙烯醇( )与丁醛缩合脱水得到的含有六元环的高分子化合物,若已知反应:CH3OH+HCHO
)与丁醛缩合脱水得到的含有六元环的高分子化合物,若已知反应:CH3OH+HCHO CH3OCH2OCH3+H2O可以发生.
CH3OCH2OCH3+H2O可以发生.
请写出制取聚乙烯缩丁醛粘合剂的化学方程式_____________________
400K,1.01×105 Pa时,2L烃A的蒸气能在m L氧气中完全燃烧,反应后体积增至(m + 4)L(体积在同前的条件下测定)。
(1)烃A在组成上应满足的条件是____________________。
(2)当m = 15时,该烃可能的分子式为__________________。
(3)若A在常温常压下为气态,m的取值范围是__________________。
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) 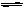 CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
| t/℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=。
(2)该反应为反应(填“吸热”“放热”)。
为体现绿色世博、低碳世博、科技世博,上海世博会已经开始使用中国自己生产的燃料电池汽车,该车以氢气和空气中的氧气为燃料,KOH为电解质溶液,真正实现了“零排放”。该电池的负极反应式为,从能量角度分析氢气用作燃料电池与直接燃烧相比主要优点是。