保护环境已成为当前和未来的一项全球性重大课题。为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图所示: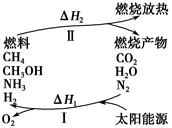
过程Ⅰ可用如下反应表示:
①2CO2 2CO+O2 ②2H2O===2H2+O2 ③2N2+6H2O
2CO+O2 ②2H2O===2H2+O2 ③2N2+6H2O 4NH3+3O2 ④2CO2+4H2O
4NH3+3O2 ④2CO2+4H2O 2CH3OH+3O2 ⑤2CO+4H2O
2CH3OH+3O2 ⑤2CO+4H2O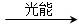 ________+3O2
________+3O2
请回答下列问题:
(1)过程Ⅰ的能量转化形式为________能转化为________能。
(2)请完成第⑤个反应的化学方程式:____________________。
(3)上述转化过程中,ΔH1和ΔH2的关系是________。
(4)断裂1 mol化学键所需的能量见下表:
| 共价键 |
H—N |
H—O |
N≡N |
O===O |
| 断裂1 mol化学键所需能量/(kJ·mol-1) |
393 |
460 |
941 |
499 |
常温下,N2与H2O反应生成NH3的热化学方程式为_________。
以下一些氧化物和单质之间可发生如右图所示的反应:其中,氧化物(Ⅰ)是红棕色固体,氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体。
(1)氧化物(Ⅰ)的化学式(分子式)是 。氧化物(Ⅱ)的化学式(分子式)是 。
(2)反应①的化学方程式是 。反应②的化学方程式是 。反应③的化学方程式是 。
(7分)化工行业已合成出一种硬度比金刚石还大的晶体——氮化碳。已知氮化碳中氮元素的化合价为-3,则:
(1)它的化学式是 。
(2)其晶体属于 晶体。
(3)你认为其硬度比金刚石大的主要原因是 。
下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
(1)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图___________。
(2)由以上元素形成的金属单质中,熔点最低的是___________________。
(3)NH3·H2O的电离方程式为NH3·H2O
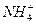 +OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______________________。
+OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______________________。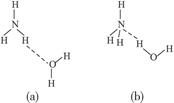
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是_________________________。(填写字母)
(5)利用稀有气体化合物,人们实现了许多制备实验上的突破。如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe。写出上述反应方程式:_____________________。
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号______________;D的原子结构示意图______________。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是_______________________。
(3)A、B、C、D形成的化合物B2A2、CD2、D2A、DA2中各原子都满足最外层8电子结构的是______________(填写具体的化学式 )。
(4)CA2与D元素的单质在水溶液中反应的化学方程式是______________________________。
已知A元素核外K、L电子层的电子总数与M、N电子层的电子总数相等,B元素的一种单质是自然界中硬度最大的物质。回答下列问题:
(1)A的元素符号为_________,B的元素符号为_________。
(2)在电弧作用下,A的氧化物能与B的单质反应,生成AB2和一种能与人体的血红蛋白结合的气体。写出AB2与水反应生成气体C的化学方程式:_____________________________。