白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
(1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1
P(s,红磷)+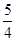 O2(g)===
O2(g)===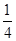 P4O10(s) ΔH2=-738.5 kJ·mol-1
P4O10(s) ΔH2=-738.5 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为________________。
(2)已知298 K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)===P4O6(s)
ΔH=-1 638 kJ·mol-1。在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________,反应过程中放出的热量为________。
已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能
(kJ·mol-1):P—P 198,Cl—Cl 243,P—Cl 331。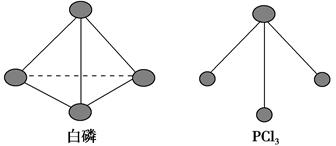
则反应P4(s,白磷)+6Cl2(g)===4PCl3(s)的反应热ΔH=________。
下图为原电池的示意图。请回答: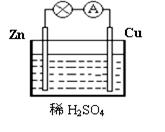
(1)Zn极为原电池的(填“正”或“负”)极,该极的电极反应式是,属于(填“氧化反应”或“还原反应”)。
(2)(填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从(填“锌片”或“铜片”)获得电子
写出下列反应的方程式 (1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(2)苯与液溴在催化剂条件下反应的化学方程式为。
(3)写出苯与氢气反应反应方程式
有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和C原子最外层只有一个电子,C燃烧时的焰色反应是黄色,C的单质在高温下与B的单质充分反应可以产生淡黄色固态化合物,A单质与D单质可以发生化合反应,且反应条件可以是点燃或者光照,试根据以上叙述回答:
写出A、B、C、D的元素名称:A _______ B _______ C _______ D ______。
(1)①葡萄糖②淀粉两种物质中,在加热条件下,与新制的氢氧化铜悬浊液加热后产生砖红色沉淀的是(填序号,下同);遇碘变蓝的是。
(2)①乙烯②乙醇③乙酸④蛋白质四种物质中,能使紫色石蕊试液变红的是(填序号,下同);能使酸性重铬酸钾由橙红色变成绿色的液体是;遇浓硝酸变黄的是通常产量可用于衡量一个国家石油化工发展水平的标志是________。
按要求写出下列有机化学反应方程式,每个3分
(1)乙醇在浓硫酸的作用下,加热到170℃时的反应方程式;
(2)乙醇在银与氧气的作用下,加热时的反应方程式;
(3)在苯酚浑浊的水溶液里,滴加氢氧化钠溶液至澄清的方程式;
(4)在苯酚钠的澄清溶液中,通入二氧化碳气体,溶液又变浑浊的方程式;
(5)在苯酚的稀溶液里滴加饱和的溴水,有白色沉淀产生的方程式;
(6)在加热的条件下,溴丙烷与氢氧化钠的水溶液反应的方程式。