25 ℃时,Kw =1.0×10-14;100 ℃时,Kw =5.5×10-13。下列说法正确的是( )
| A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 |
| B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 |
| C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L CH3COOH恰好中和,所得溶液的pH="7" |
| D.25 ℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
下列现象或事实可用同一原理解释的是
| A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 | B.氯水和活性炭使红墨水褪色 |
| C.漂白粉和钠长期暴露在空气中变质 | D.氯水和过氧化钠使品红褪色 |
已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是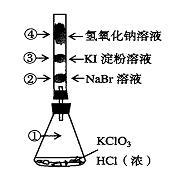
| ① |
② |
③ |
④ |
|
| A |
黄绿色 |
橙色 |
蓝色 |
无色 |
| B |
无色 |
橙色 |
紫色 |
白色 |
| C |
黄绿色 |
橙色 |
蓝色 |
白色 |
| D |
黄绿色 |
无色 |
紫色 |
白色 |
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是
| A.①②③④ | B.①②⑤⑥ | C.③⑤⑥⑦ | D.①③④⑦ |
下列说法正确的是
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧 化物 化物 |
| B.蔗糖、硫酸钡和水分别属于非电解质、弱电解质和弱电解质 |
| C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源 |
下列说法正确的是
| A.可用丁达尔现象区分溶液与胶体 | B.生石灰与水混合的过程只发生物理变化 |
| C.O3是由3个氧原子构成的化合物 | D.CuSO4·5H2O是一种混合物 |