Al、Fe、Cu都是重要的金属元素。下列说法正确的是( )
| A.三种金属单质在常温下均可溶于浓硫酸 |
| B.三种金属单质放置在空气中均只能生成氧化物 |
| C.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
| D.制备AlCl3、FeCl3、CuCl2三种固体物质,均不能采用将溶液直接蒸干的方法 |
下列实验所用试剂、现象和结论均正确的是:
| 序号 |
实验内容 |
试剂 |
现象和结论 |
| ① |
鉴别K2CO3和Na2SO3 |
盐酸、澄清的石灰水 |
产生无色无味气体,能使澄清的石灰水变浑浊的是K2CO3 |
| ②[ |
鉴别NO2和Br2蒸气 |
湿润的淀粉KI试纸 |
试纸变蓝色的是Br2蒸气 |
| ③ |
除去氯化钙溶液中的氯化铁杂质 |
生石灰 |
调节溶液的pH为3.7,再过滤 |
| ④ |
鉴别AlCl3溶液和MgCl2溶液 |
氨水 |
产生白色沉淀然后消失的是AlCl3溶液 |
A.①③ B.①②③C.②④ D.①②③④
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
| 序号 |
甲 |
乙 |
丙 |
| ① |
CO2 |
SO2 |
石灰水 |
| ② |
HCl |
CO2 |
石灰水 |
| ③ |
CO2 |
SO2 |
Ba(NO3)2 |
| ④ |
NO2 |
SO2 |
BaCl2 |
| ⑤ |
CO2 |
NH3 |
CaCl2 |
A.②③④B.①②③④C.①③④ D.②③④⑤
SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕黄色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化,下列说法不正确的是
| A.上述过程中,最终被还原的是NO3— |
| B.从上述反应可以得出结论,氧化性:HNO3>Fe3+>稀硫酸 |
| C.上述过程中,会产生一种无色难溶于水的气体 |
| D.假设通入的 SO2完全反应,则同温同压下,SO2和逸出气体的体积比为 1∶1 |
饱和氯水中存在如下平衡:①Cl2+H2O H++Cl-+HClO ;②HClO
H++Cl-+HClO ;②HClO H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是()
H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是()
| A.加入CaCO3悬浊液,CaCO3的溶解平衡向右移动 |
| B.加入澄清石灰水,c(H+)一定减小 |
| C.加入一定量NaOH溶液后,溶液中离子浓度的关系可能为c(Cl-) +c(ClO-) =c(Na+) |
| D.通入过量Cl2,①、②均向右移动,溶液pH减小 |
若氧元素只有16O、18O两种核素,下列说法正确的是
| A.16O和18O的物理性质和化学性质完全相同 |
| B.通过化学反应可以实现16O与18O的相互转化 |
C.向2SO2(g)+ O2(g)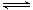 2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中 2SO3(g)的平衡体系中加入18O2,达到新的平衡后18O只出现在O2与SO3中 |
| D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子 |