短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是 ( )。
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.含Y元素的盐溶液有的显酸性,有的显碱性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3KJ/mol
已知CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)ΔH=-Q1KJ/mol
1/2H2SO4(浓)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)ΔH=-Q2KJ/mol
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)ΔH=-Q3KJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为()
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |
N2O5是一种新型硝化剂。其性质和制备受到人们的关注。一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g) 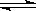 4NO2(g)+O2(g)ΔH>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是()
4NO2(g)+O2(g)ΔH>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是()
| A.20s内平均反应速率V(N2O5)=0.1mol·(L·s)-1 |
| B.10s时,正逆反应速率相等,达到平衡 |
| C.20s时,正反应速率大于逆反应速率 |
| D.曲线a表示NO2的物质的量随反应时间的变化 |
反应PCl5(g) PCl 3(g)+Cl2(g) ① 2HI(g)
PCl 3(g)+Cl2(g) ① 2HI(g) H2(g)+I2(g) ②
H2(g)+I2(g) ②
2NO2(g) N2O4(g)③
N2O4(g)③
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率()
| A.均不变 | B.均增大 | C.①增大,②不变,③减少 | D.①减少,②不变,③增大 |
在恒温时,一固定容积的容器内发生如下反应:2NO2(g) N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数()
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数()
| A.不变 | B.增大 | C.减小 | D.无法判断 |
下列说法正确的是( )
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |