甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)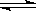 CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g)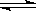 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
①上述反应符合“原子经济”原则的是________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 |
250 ℃ |
300 ℃ |
350 ℃ |
| K |
2.041 |
0.270 |
0.012 |
由表中数据判断,ΔH1______0(填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为________(从上表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)=H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________________________________。
I.由C、H、O三种元素组成的有机物R,R的相对分子质量122,其中含碳元素的质量分数为68.9%,含氧元素的质量分数为26.2%。R与NaHCO3溶液反应,生成的气体能使澄清石灰水变浑浊。则R的分子式是____________________。
II.M是生产某新型塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(图中球与球之间连线代表化学键单键或双键等)。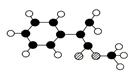
拟从芳香烃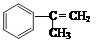 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
已知:M在酸性条件下水解生成有机物F和甲醇。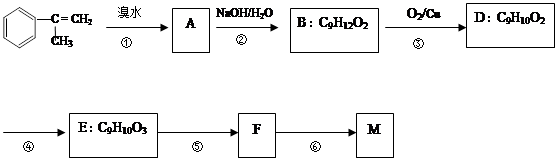
(1)M的结构简式。
(2)写出②、⑤反应类型分别为、。
(3)D中含氧官能团的名称为,E的结构简式。(4)写出反应⑥的化学方程式(注明必要的条件):
。
(5)写出符合下列两个条件的结构简式:①与F互为同分异构体;②能发生水解反应,水解产物有两种,一种能使溴的四氯化碳溶液褪色,另一种滴加FeCl3溶液显紫色。。
由两种元素组成的化合物A存在如下图所示的转化关系(部分产物及反应条件已略去)。已知:E为红棕色气体,F、H为金属单质,J为黑色非金属单质。L露置于空气中时,由白色最终转化为红褐色,B与F反应时可生成C,也可生成G。试回答下列问题: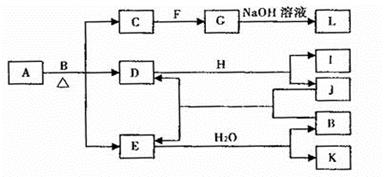
(1)物质K的名称是_________;I的晶体属于____________晶体。
(2)已知A中两种元素原子成最简整数比,且金属元素与非金属元素的质量比为14:1,则A的化学式为 。
(3)写出下列反应的化学方程式:
L露置于空气中时,由白色最终转化为红褐色____________。
A与B反应的化学方程式___________。
(4)H在D中燃烧的现象为____________。
(5)若各步反应都看成是进行完全的,则当生成a mol物质L时,需要A_________mol。
有机化合物与人类日常生活密不可分,下面有几种常见食品
花生油鸡蛋米饭
(1)花生油中所含人体需要的主要营养物质为(填“糖类”、“油脂”、或“蛋白质”),人体摄入花生油后,在体内酶的催化作用下反应生成高级脂肪酸和。
(2)吃饭时,咀嚼米饭一会儿后感觉有甜味,这是因为淀粉在唾液淀粉酶的作用下发生了
反应。(选填下列选项编号)
| A.分解 | B.水解 | C.加成 | D.酯化 |
2.16g某有机物在纯氧中完全燃烧,依次通入装有无水氯化钙的干燥管、盛有足量澄清石灰水的洗气瓶,结果无水氯化钙干燥管增重1.44g,通过澄清石灰水得到沉淀14g。又知此有机物蒸气0.224L(已折算成标准状况下)的质量为1.08g。
⑴求此有机物的分子式。
⑵若此有机物跟FeCl3溶液作用显紫色,写出此有机物可能的结构简式。
X是一种可用作果实催熟剂的气体。现有如下的反应关系: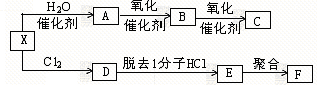
已知F是合成高分子化合物,用于制备塑料和合成纤维。
(1)用结构简式表示:A、C、F;
(2) A→B的化学方程式为,反应类型为。