900 ℃时,向2.0 L恒容密闭容器中充入0.40 mol乙苯,发生反应: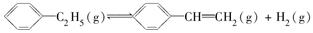 ΔH=a kJ·mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ·mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| 时间/min |
0 |
10 |
20 |
30 |
40 |
| n(乙苯)/mol |
0.40 |
0.30 |
0.24 |
n2 |
n3 |
| n(苯乙烯)/mol |
0.00 |
0.10 |
n1 |
0.20 |
0.20 |
下列说法正确的是( )。
A.反应在前20 min的平均速率为v(H2)=0.008 mol·L-1·min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08 mol·L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10 mol乙苯、0.10 mol苯乙烯和0.30 mol H2,达到平衡前v正>v逆
同位素示踪法可用于反应机理的研究,下列反应中同位素示踪表示正确的是()
| A.2Na218O2 + 2H2O ="=" 4Na18OH + O2↑ |
| B.2KMnO4 + 5H218O2 + 3H2SO4 ="=" K2SO4 + 2MnSO4 + 518O2↑ + 8H2O |
C.NH4Cl + 2H2O NH3·2H2O + HCl NH3·2H2O + HCl |
| D.K37ClO3 + 6HCl ="=" K37Cl + 3Cl2 ↑+ 3H2O |
用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 |
操作及现象 |
溶液 |
| A |
通入CO2,溶液不变浑浊.先通入CO2再通入氨气,溶液变浑浊 |
CaCl2溶液 |
| B |
通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. |
Na2SiO3溶液 |
| C |
通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. |
Ca(ClO)2溶液 |
| D |
通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. |
Ca(OH)2溶液 |
有15mL 2mol·L-1的H2SO4溶液与15mL 3 mol·L-1的Na2CO3溶液,欲使其反应产生CO2的量最多,则正确的操作是()
| A.把两种溶液快速混合并不断搅拌 | B.把两种溶液缓慢混合并不断搅拌 |
| C.把Na2CO3溶液滴加到H2SO4溶液中 | D.把H2SO4溶液滴加到Na2CO3溶液中 |
在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3。铜粉可溶解的是 ( )
| A.①② | B.②④ | C.②③ | D.①④ |
下列有关铁元素的叙述中正确的是()
| A.Fe(OH)2易被氧化成Fe(OH)3,说明稳定性:Fe(OH)2 < Fe(OH)3 |
| B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI=FeI3+3H2O |
| D.铁元素位于周期表的第四周期第VIIIB族 |