25 ℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述,正确的是 ( )。
| A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32—)+c(OH-)+c(Cl-) |
| B.pH=4的溶液中:c(H2CO3)+c(HCO3—)+c(CO32—)<0.1 mol·L-1 |
| C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3—)=c(OH-)+c(Cl-) |
| D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32—)>c(HCO3—)>c(H2CO3) |
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O =3I 2+6OH- |
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.将过量二氧化硫气体通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++3NO3-=Ag++3NO↑+H2O |
下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是
| A.a-b-c-d-e-e-f-g-h | B.a-e-d-c-b-h-i-g | C.a-d-e-c-b-h-i-g | D.a-c-b-d-e-h-i-f |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是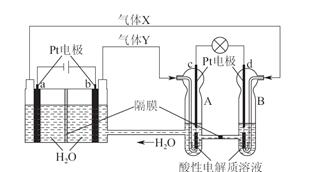
A.转移0.1mol电子时,a电极产生1.12LH2
B.b电极上发生还原反应
C.酸性电解质溶液中H+移向c电极
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
有一种纸质软电池,该电池采用薄层纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法正确的是
| A.该电池Zn为负极,ZnO为正极,MnO2催化剂] |
| B.该电池的正极反应为MnO2+e-+H2O=MnO(OH)+OH- |
| C.放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D.电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动 |
某溶液可能含有Cl–、SO42–、CO32–、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤、洗涤、灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.Cl– 一定存在,且c(Cl–)≥0.4mol/L |
| C.SO42–、NH4+一定存在,Cl–可能不存在 |
| D.CO32–、Al3+一定不存在,K+可能存在 |