某温度(t ℃)时,水的离子积为KW=1.0×10-13mol2·L-2,则该温度(填“大于”、“小于”或“等于”)________25 ℃,其理由是_______________________________________。
若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
(1)若所得混合液为中性,则a∶b=________;此溶液中各种离子的浓度由大到小排列顺序是___________________________________。
(2)若所得混合液的pH=2,则a∶b=________。此溶液中各种离子的浓度由大到小排列顺序是__________________________________________。
溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,
⑴、该溶液中肯定含有的离子是,且各离子的物质的量之比为;肯定不含的离子是。
⑵、还有一种离子可能存在,写出检验这种离子的实验方法及现象:
。
(1)油脂被摄入人体后,在酶的作用下水解为和甘油(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)发育出现障碍,患营养缺乏症,这主要是由于摄取_________(填“蛋白质”、“脂肪”或“糖类”)不足引起的。下列食物中富含该物质的是(填字母)。
| A.菠菜 | B.花生油 | C.瘦肉 | D.西瓜 |
(3)某品牌抗酸药的成分主要有糖衣、碳酸钙、淀粉等。
①写出该抗酸药发挥功效时的离子方程式:。
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,写出其水解方程式:。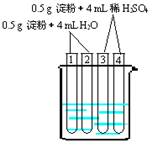
(4)上图所示4支试管同时水浴加热4min,为检验其中淀粉的水解程度,某同学的实验操作与现象记录如下:
| 编号 |
操作 |
现象 |
| 1 |
加入碘水 |
溶液变成蓝色 |
| 2 |
加入银氨溶液,水浴加热 |
未出现银镜 |
| 3 |
加入碘水 |
溶液变成蓝色 |
| 4 |
加入银氨溶液,水浴加热 |
未出现银镜 |
①结合试管1、2中的现象,得出的结论是,这两支试管中淀粉水解(填“没有”、“部分”或“全部”)。
②结合试管3、4中的现象,不能得出“这两支试管中淀粉没有水解”的结论,理由是
。
防治环境污染,改善生态环境己成为全球的共识。
(1)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有(填字母)标志的垃圾筒内。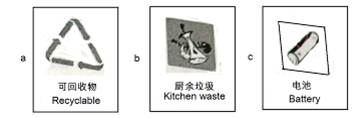
(2)工业废水需处理达标后才能排放。下列废水处理的方法合理的是(填字母)。
a.用中和法除去废水中的酸
b.用混凝法除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
d.用氧化还原法除油类、氰化物
(3)为了减少煤燃烧产生的SO2对大气造成的污染,可向煤中加入适量石灰石。石灰石与煤燃烧时产生的SO2及空气中的O2反应,生成CaSO4和CO2,写出该反应的化学方程式:。
某芳香烃A有如下转化关系: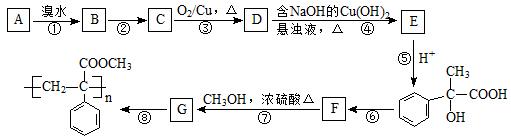
按要求填空:
⑴写出反应②和⑥的反应条件:②;⑥。
⑵写出A和G结构简式:A;G。
⑶写出反应③对应的化学方程式:;
⑷写出反应⑦对应的化学方程式:。
⑸属于取代反应的有(填序号),反应⑧的反应类型属于。
通过下列实验比较① ② CH3CH2OH ③ H-OH④
② CH3CH2OH ③ H-OH④
⑤ 五种物质中羟基上氢原子的活泼性顺序。在下表中填写实验现象及实验结论。
五种物质中羟基上氢原子的活泼性顺序。在下表中填写实验现象及实验结论。
| 编号 |
实验操作 |
实验现象 |
实验结论 |
| 1 |
分别取上述五种物质的少量溶液或液体于试管中,各滴入几滴石蕊试液 |
||
| 2 |
分别取适量①、⑤的水溶液,各加入少量NaHCO3固体 |
||
| 3 |
分别取少量②、③、④,各加入适量NaOH溶液,再通入足量CO2 |
||
| 4 |
分别取少量②、③的液体,各加入一小粒金属钠 |
结论:上述五种物质中的羟基上氢原子活泼性顺序为(填序号)