在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中,加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目几乎没有变化的是
| A.Fe3+ | B.Al3+ | C.NH4+ | D.Fe2+ |
下列表达式错误的是:
A.甲烷的电子式: |
B.氮原子的L层电子的电子排布图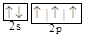 |
| C.硫离子的核外电子排布式:1S22S22P63S23P4 |
D.碳-12原子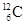 |
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是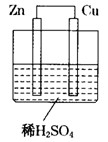
实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO 向Cu极移动
向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu-2e-===Cu2+,发生氧化反应
| A.①②③ | B.②④ | C.②③④ | D.③④⑤ |
将4molA气体和2molB气体置于2L的密闭容器中,混合后发生如下反应:
2A(g) + B(g) 2C (g) 。若经2s后测得C的浓度为 0.6mol/L ,下列说法正确的是
2C (g) 。若经2s后测得C的浓度为 0.6mol/L ,下列说法正确的是
| A.用物质A表示的反应速率为0.6mol/(L·s) |
| B.用物质B表示的反应速率为0.3mol/(L·s) |
| C.2s时物质B的浓度为0.3mol/L |
| D.2s时物质A的转化率为30% |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性: W>R |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
下列表述正确的是
A.用电子式表示氯化氢分子的形成过程: |
B.2CH3CH2OD+O2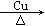 2CH3CHO+2DHO 2CH3CHO+2DHO |
| C.乙醇的结构简式C2H6O |
D.实验室中制取乙酸乙酯的方程式为:CH3COOH+H18O-C2H5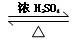 CH3COOC2H5+H218O CH3COOC2H5+H218O |