有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 |
K+、Na+、Al3+、Cu2+ |
| 阴离子 |
OH-、HCO3-、NO3-、SO42- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象。
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:B ; C 。
(2)写出过量E滴人到C溶液中的离子反应方程式 。
(3)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 。
(4)在A溶液中加澄清石灰水,其离子方程式为 。
(5)上述五种化合物中有一种是常用作净水剂,其净水原理是: (请结合方程式及必要的文字进行叙述)。
下列是中学化学中常见物质间的反应转化关系图,其中部分产物已略去,常温下,G为固体单质,B、I为液体,其余都为气体.A为化合物,I的浓溶液与G在加热条件下生成F、B和C。 H可用作工业上冶炼金属的还原剂。请按要求填空:
(1)写出下列物质的化学式:A:________;B:________;C:________.
(2)写出F+B→I的化学方程式_________________________________.
(3)写出G和I的浓溶液反应的化学方程式_________________________
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:(1)氮元素原子的L层电子数为__________;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_________________________;
(3) 肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为________________________________。
Ⅱ、一定质量的液态化合物XY2在标准状况下的一定质量的O2中恰好完全燃烧,反应方程式为: XY2(l)+3O2 (g) ="==" XO2(g)+2YO2 (g)冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56g/L则: (1)反应前O2的体积是________。(2)化合物XY2的摩尔质量是___________。
(3)XY2分子中X、Y两元素质量比是3∶16, X、Y两元素分别为__________ (写元素符号)。
邻羟基桂皮酸是合成香精的重要原料,下为合成邻羟基桂皮酸的路线之一:
试回答下列问题:
(1)化合物III 在银氨溶液中发生反应化学方程式:;
(2)有机物 X 为化合物IV的同分异构体,且知有机物X 有如下特点:
①是苯的对位取代物,②能与NaHCO3反应放出气体,③能发生银镜反应。
请写出化合物X的结构简式;
(3)下列说法正确的是;
| A.化合物I遇氯化铁溶液呈紫色 | B.化合物II能与NaHCO3溶液反应 |
| C.1mol化合物IV完全燃烧消耗 9.5molO2 | D.1mol化合物III最多能与3 molH2 反应 |
(4)有机物R(C9H9ClO3)经过反应也可制得化合物IV,则 R 在NaOH 醇溶液中反应的化学方程式为。
有机物A有下列转化关系,已知等物质的量的B和C完全燃烧后产生的CO2的量相等。
|


|
请回答:
(1)物质A和B的结构简式分别是__ __。(每个1分,共2分)有以下一系列反应,最终产物为草酸。已知B的相对分子质量比A大79。
A B
B C
C  D
D  E
E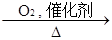 F
F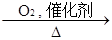 乙二酸(也叫草酸,分子式为C2H2O4)
乙二酸(也叫草酸,分子式为C2H2O4)
(1)B→C的转化条件是(1分)
(2)写出下列转化的化学方程式 (方程式每个2分,共8分)
① A→B ;
② D→E ;
③ E→F;
④E与乙二酸在某条件下1:1反应生成有机环状物;